地氯雷他定干混懸劑
其他H1受體阻斷葯
地氯雷他定干混懸劑,適應症為用於緩解慢性特發性蕁麻疹及常年性過敏性鼻炎的全身及局部癥狀。
本品主要成份為地氯雷他定。
化學結構式:
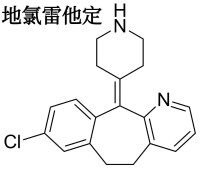
地氯雷他定干混懸劑
分子量:310.82
本品為類白色至淺粉色粉末狀顆粒或粉末,味甜。
用於緩解慢性特發性蕁麻疹及常年性過敏性鼻炎的全身及局部癥狀。
(1)0.5 g:2.5 mg(以地氯雷他定計); (2)1 g:5 mg(以地氯雷他定計)
(1)0.5 g:2.5 mg
1~5歲兒童:口服,每日一次,每次半袋(1.25 mg)。
6~11歲兒童:口服,每日一次,每次1袋(2.5 mg)。
成人和青少年(12歲或12歲以上):口服,每日一次,每次2袋(5 mg)。
溶於水中,服用前攪拌均勻,地氯雷他定可與食物同時服用。
(2)1 g:5 mg
1~5歲兒童:口服,每日一次,每次1/4袋(1.25 mg)。
6~11歲兒童:口服。每日一次,每次半袋(2.5 mg)。
成人和青少年(12歲或12歲以上):口服,每日一次,每次1袋(5 mg)。
溶於水中,服用前攪拌均勻,地氯雷他定可與食物同時服用。
在患兒的臨床試驗中,246例6個月至11歲的患兒服用地氯雷他定糖漿,2~11歲年齡組其不良事件的總發生率與安慰劑相似。在6個月至2歲年齡組,最常見的並且高於安慰劑組的不良事件為腹瀉(3.7%)、發熱(2.3%)和失眠(2.3%)。
在一系列以過敏性鼻炎和慢性特發性蕁麻疹為適應症的臨床試驗中,患者按每天5毫克的推薦劑量服用地氯雷他定,試驗組不良反應的發生率比安慰劑組高出3%。超過安慰劑組的最常見不良反應為疲倦(1.2%)、口乾(0.8%)和頭痛(0.6%)。
對本品活性成份或輔料過敏者禁用。
2)嚴重腎功能不全患者慎用;
由於尚無孕婦使用地氯雷他定的臨床資料,懷孕期內使用地氯雷他定的安全性尚未確定,除非潛在的益處超過可能的風險,懷孕期內不應使用地氯雷他定。
地氯雷他定可經乳汁排泌,因此不建議哺乳期婦女服用地氯雷他定。
給予34倍人體臨床推薦劑量的地氯雷他定,未發現對大鼠的總體生育能力有影響。在動物試驗中未發現地氯雷他定有致畸變和致突變作用。
地氯雷他定對1歲以下的兒童患者的療效和安全性尚未確定。
尚缺乏老年患者用藥的研究資料。
臨床試驗中未發現地氯雷他定存在有臨床相關意義的相互作用。地氯雷他定在與阿奇黴素、酮康唑、紅黴素、氟西汀和西咪替丁的多劑量藥物相互作用試驗中,血漿濃度未出現有臨床相關意義的改變。然而地氯雷他定的代謝酶尚未確定,因此與其他藥物的相互作用尚不能完全排除。
地氯雷他定與其他抗交感神經葯或有中樞神經系統鎮靜作用的葯合用會增強睡眠。
進食與飲用葡萄柚果汁對地氯雷他定的分佈無影響。
地氯雷他定與酒精同時使用時不會增強酒精對人行為能力的損害作用。
服藥過量時應考慮採取標準治療措施去除未吸收的活性物質。建議進行對症及支持治療。
在一項對成人和青少年進行的多劑量臨床試驗中,受試者接受高達45 mg的地氯雷他定(臨床實際用量的9倍),未見臨床相關不良反應。
藥理作用
本品為非鎮靜性的長效三環類抗組胺葯,為氯雷他定的活性代謝物,可通過選擇性地拮抗外周H1受體,緩解季節性過敏性鼻炎或慢性特發性蕁麻疹的相關癥狀。另外,體外研究結果表明,本品可抑制組胺從人肥大細胞釋放。動物研究提示,本品不易通過血腦屏障。
毒理研究
急性毒性:本品經口給藥劑量達250 mg/kg時出現死亡(按AUC計算,地氯雷他定及其代謝產物的暴露量約為臨床推薦日口服劑量的120倍),小鼠經口給葯LD50為353 mg/kg(按體表面積計算,地氯雷他定約為臨床推薦劑量的290倍)。猴經口給藥劑量達250 mg/kg(按體表面積計算,地氯雷他定約為臨床推薦劑量的810倍)時,未出現死亡。
生殖毒性:本品經口給藥劑量達24 mg/kg/日(地氯雷他定及其代謝物的暴露量約為臨床日推薦口服劑量下AUC的130倍)時,對雌性大鼠生育力無影響;經口給藥劑量達12 mg/kg/日(地氯雷他定及其代謝物的暴露量約為臨床日推薦口服劑最下AUC 45倍)時,出現雌鼠受孕率下降、雄鼠精子數減少、精子活力降低和睾丸組織學改變,表明雄性大鼠生育力降低;經口給藥劑量為3 mg/kg/日(地氯雷他定及其代謝物的暴露量約為臨床日推薦口服劑量下AUC的8倍)時,對大鼠生育力無影響。
大鼠和家兔經口給予本品,劑量分別達48和60 mg/kg/日(地氯雷他定達到及其代謝物的暴露量分別約為臨床日推薦口服劑量下AUC的210和230倍)時,未見致畸作用。雌性大鼠給藥劑量為24 mg/kg/日(地氯雷他定及其代謝物的暴露量約為臨床日推薦口服劑量下AUC的120倍)時,可見植入前丟失率增加、植入數和胚胎數減少;給藥劑量為9 mg/kg/日(地氯雷他定及其代謝物的暴露量約為臨床日推薦口服劑量下AUC的50倍)或以上時,可見仔鼠體重減輕和翻正反射減慢;給藥劑量為3 mg/kg/日(地氯雷他定及其代謝物的暴露量約為臨床日推薦口服劑量下AUC的7倍)時,本品對仔鼠發育無影響。
致癌性:通過氯雷他定的研究對本品的潛在致癌性進行了評估。小鼠和大鼠分別連續經口給予氯雷他定18個月和2年,雄性小鼠給藥劑量達40 mg/kg/日(地氯雷他定及其代謝物的暴露量約為臨床日推薦口服劑量下AUC的3倍)時,肝細胞瘤(包括腺瘤和癌)的發生率明顯高於對照組。雄性大鼠給藥劑量為10 mg/kg/日,雌性和雄性大鼠給藥劑量為25 mg/kg/日(地氯雷他定及其代謝物的暴露量約為臨床日推薦口服劑量下AUC的7和30倍)時,肝細胞瘤發生率顯著升高。以上發現與地氯雷他定長期給葯的臨床相關性尚不明確。
未針對地氯雷他定對兒童的有效性進行單獨的臨床試驗。兩項兒科臨床試驗對其安全性進行了評價。接受抗組胺治療的1個月~11歲患兒,每日劑量1.25 mg(1~5歲患兒)或2.5 mg(6~11歲患兒),通過臨床檢查、生命體征和ECG檢查(包括QT間期),證明其耐受性良好。給予推薦劑量時,兒科和成人群體的地氯雷他定血漿濃度是可比的(見葯代動力學)。
成人患者和患兒的季節性過敏性鼻炎(SAP)/慢性特發性蕁麻疹(CIU)病程和地氯雷他定藥理葯代特點是相似的,因此地氯雷他定對成人群體的療效可以外推到兒童群體。
地氯雷他定不易透過中樞神經系統。在推薦劑量5毫克/日下,嗜睡反應發生率與安慰劑相似。臨床試驗中,即使在7.5毫克/日的劑量下,地氯雷他定也不會影響智力操作技能。單劑量服用地氯雷他定5 mg對飛行能力的標準量度,包括嗜睡的加劇或有關飛行的任務無影響。
臨床藥理學試驗中,地氯雷他定與酒同服並不增加酒精所引起的行為能力的損害和嗜睡。無論是單獨服用還是與酒同服,地氯雷他定組和安慰劑組在精神運動試驗方面均無顯著差別。
在兩項為期4周的對季節性過敏性鼻炎併發哮喘患者進行的臨床試驗中,地氯雷他定能有效緩解季節性過敏性鼻炎的癥狀(流涕、鼻塞、鼻癢及打噴嚏;眼癢及燒灼感;流淚;充血;齶癢及耳癢)及哮喘的癥狀(咳嗽、喘鳴及呼吸困難),並能減少β受體激動劑的用量。地氯雷他定組和安慰劑組的第一秒用力呼氣量(FEVI)均未改變。
在對慢性特發性蕁麻疹成人和青少年患者進行的臨床試驗中,服用本品1天後即可緩解瘙癢並減少蕁麻疹的數量及大小。在各項研究中,地氯雷他定在24小時的服藥間隔內能夠維持療效。服用地氯雷他定能夠減少嗜睡對日間生活的影響,提高患者睡眠及日常生活的質量。
對過敏性鼻-結膜炎患者的問卷調查表明,地氯雷他定能夠有效緩解季節性過敏性鼻炎患者的病情,能夠顯著改善癥狀所造成的日常不便。
地氯雷他定口服后30分鐘可測得其血漿濃度,吸收較好,約3小時后可達血葯峰濃度。終末半衰期約為27小時。地氯雷他定的蓄積程度與其半衰期(約27小時)及每日一次的服藥間隔一致。成人和青少年地氯雷他定的生物利用度在5 mg~20 mg範圍內與劑量成正比。
尚未確立地氯雷他定代謝對酶的依賴性,因不完全排除其與其他藥物間的相互作用。與CYP3A4和CYP2D6的特異性抑製劑的體內試驗表明,這些酶在地氯雷他定的代謝中並不重要。地氯雷他定不抑制CYP3A4或CYP2D6,而且也不是P-糖蛋白的底物或抑製劑。
幾項獨立的單劑量研究結果顯示,在推薦的劑量下,患兒的AUC和Cmax值與服用5 mg地氯雷他定糖漿劑的成人具有可比性。
密閉,陰涼(不超過20°C)乾燥處保存。
複合膜雙鋁包裝,3袋/盒、6袋/盒、8袋/盒、10袋/盒、12袋/盒、14袋/盒、16袋/盒、18袋/盒、20袋/盒。
36個月
國家食品藥品監督管理局標準(試行)YBH11622004
2021年8月22日,普利製藥發布公告,公司的地氯雷他定干混懸劑順利通過荷蘭藥物評價委員會和德國聯邦藥物和醫療器械管理局的審評,不日即將獲得荷蘭和德國的上市許可。
