氨基糖甙類
氨基糖甙類
主要包含的抗生素:鏈黴素、慶大黴素、慶大黴素珠鏈、卡那黴素、丁胺卡那黴素、雙去氧卡那黴素、復方卡那黴素注射液、卡那黴素B、妥布黴素西梭黴素、奈替米星核糖黴素巴龍黴素、青紫黴素、小諾黴素、新黴素阿司黴素、淋必治、異帕米星。
1.源自鏈黴菌的氨基糖苷類藥物
1943年,從放線菌屬灰鏈絲菌的培養液中提取到後用於治療結核病的鏈黴素,此後繼續發的新黴素(1949年)、卡那黴素(1957年)以及用於治療原蟲感染的巴龍黴素(1965年)、抗銅綠假單胞菌活性較強的妥布黴素(1970年)、廣泛獸用的安普黴素(1970年)、用於輕度感染的核糖黴素(1970年)、用於治療淋病的大觀黴素(1971年)和利維黴素(1972年)都是從鏈黴菌中提取的天然氨基糖苷類藥物。
首個半合成氨基糖苷類藥物阿米卡星(1972年)為卡那黴素A的衍生物,與新黴素、卡那黴素、核糖黴素、慶大黴素B和利維黴素相比,其對磷酸轉移酶穩定,故對假單胞菌具抗菌活性。
2.源自小單孢菌的氨基糖苷類藥物
與新黴素和卡那黴素相比,慶大黴素C(1963年)因不存在3位磷酸化的羥基,故對假單胞菌的活性更強。慶大黴素的抗菌譜較廣,抗菌活性強,價格低廉,對銅綠假單胞菌、大腸埃希菌、產氣桿菌、克雷伯菌、奇異變形桿菌、某些吲哚變形桿菌、某些奈瑟菌、某些無色素雷桿菌和志賀菌等革蘭陰性菌都有抗菌作用,且對革蘭陽性菌中的金黃色葡萄球菌(包括其耐葯株)也有很強的抗菌作用,臨床上主要用於治療革蘭陰性菌及耐葯金黃色葡萄球菌所致的嚴重感染如敗血症、呼吸道感染、尿路感染、膽道感染和燒傷感染等。
1970年發現的西索米星雖然抗菌活性優於慶大黴素,但毒、副作用也遠大於慶大黴素,故並未得到廣泛應用。后對西索米星進行結構修飾得到奈替米星(1974年),後者對部分產乙醯轉移酶的菌株有活性,動物實驗證實其耳、腎毒性比西索米星低。
異帕米星(1977年)是慶大黴素B(1971年)的1-N-HABA衍生物,具有與阿米卡星相似的抗菌活性,但對產染色體介導的乙醯轉移酶的沙雷菌作用更強,當時並未用於臨床。直至10餘年後革蘭陰性菌廣泛產染色體介導的6-乙醯轉移酶時,異帕米星才再次在美國“多學科抗微生物藥物與化療會議”上得到介紹,不久在日本和韓國上市,后又獲得某些歐洲國家的批准。異帕米星對大多數腸桿菌科細菌、假單胞菌屬、不動桿菌屬和沙門菌等革蘭陰性桿菌以及包括耐甲氧西林金黃色葡萄球菌(MRSA)在內的金黃色葡萄球菌、表皮葡萄球菌等具有良好的抗菌作用,對慶大黴素和阿米卡星敏感的腸桿菌科細菌和銅綠假單胞菌的作用較阿米卡星略強或相似,適用於治療對其它氨基糖苷類藥物、包括對阿米卡星耐葯的革蘭陰性桿菌(包括銅綠假單胞菌)和葡萄球菌所致的嚴重感染。
異帕米星具有顯著的抗生素後效應,故給藥方案被設計為一日1次400mg,既保證療效又能降低毒性。異帕米星維持並加強了氨基糖苷類藥物的優勢,具有強效殺菌活性、致耐藥性低以及毒、副作用小和有良好的抗生素後效應等特點,已成為新一代抗菌良藥,在國、內外廣泛用於各類細菌感染治療,被認為是氨基糖苷類藥物中的“王牌”。
依替米星(1997年)是我國自行開發的新葯,系以慶大黴素C1a為母核、經將其二脫氧鏈霉胺1-N位上的1個氫原子用1個乙基取代所得。臨床前及Ⅱ期臨床試驗顯示,依替米星對多種耐葯菌(包括MRSA)所致的感染均有較好的療效,且毒、副作用小,尤其是耳、腎毒性較低,總體上與奈替米星相似。體外抗菌作用研究表明,依替米星的抗菌譜廣,對多種病原菌,特別是大腸埃希菌、肺炎克雷伯菌、腸桿菌屬、沙雷菌屬、奇異變形桿菌、沙門菌屬、流感嗜血桿菌和葡萄球菌屬等都有較高的抗菌活性,對部分假單胞菌、不動桿菌屬等也具有一定的抗菌活性,對部分對慶大黴素、小諾黴素和頭孢唑啉耐葯的金黃色葡萄球菌、大腸埃希菌和肺炎克雷伯菌的體外MIC值仍在其治療劑量的血葯濃度範圍內。依替米星對產青霉素酶的部分葡萄球菌和部分低水平MRSA亦有一定的抗菌活性。依替米星克服了慶大黴素、阿米卡星等傳統氨基糖苷類藥物治療安全係數較低的缺點,毒、副作用小,是一個有競爭力的新抗菌藥物。
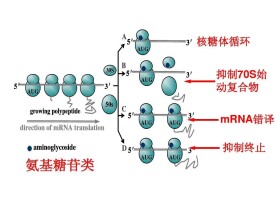
早期發現氨基糖苷類藥物是經直接作用於細菌30S核糖體亞單位、使細菌發生讀碼錯誤而最終導致細菌死亡的。近年來更加深入的研究表明,此類藥物是直接與30S核糖體亞單位的16SrRNA解碼區的A部位結合的。雖然氨基糖苷類藥物的結合點都是16SrRNA的保守區域,但它們對原核和真核核糖體的作用並不相同。
氨基糖苷類藥物屬靜止期殺菌葯,其殺菌作用具有如下特點:
1.殺菌作用呈濃度依賴性;
2.僅對需氧菌有效,尤其以對需氧革蘭陰性桿菌的抗菌作用為最強;
3.具有明顯的抗生素後效應;
4.具有首次接觸效應;
5.在鹼性環境中的抗菌活性增強。
目前按抗菌的藥效動力學將抗菌葯分為濃度依賴性和時間依賴性兩大類。濃度依賴性(Cmax/MIC,AUC24/MIC)代表性抗生素是氨基糖苷類、喹諾酮類和硝基咪唑類;時間依賴性(T>MIC)代表性抗生素為β-內醯胺類、大環內酯類、林可醯胺類、磺胺甲氧苄啶和惡唑烷酮;濃度依賴型抗菌葯的主要參數指標是:Cmax/MIC≥8~10,或AUC/MIC≥100~125時可獲良好療效,亦可防止在治療過程中產生耐葯突變株。
濃度依賴性氨基糖苷類抗生素給藥方案的選擇:藥效學取決於PD和PK相結合的濃度指標Cmax/MIC>8~12。氨基糖苷給藥方案選擇1日1次療法有利於Cmax/MIC>8~12,療效高,防止耐藥性的產生。氨基糖苷1日多次給葯(如8~12h給葯1次)是在首次暴露效應之後恰好在“適應性耐葯期”給葯,不產生殺菌作用,反而強化適應性耐葯。適應性耐葯2h開始6~16h耐藥性最高,24h藥效部分恢復。每日1次給葯,耳、腎毒性≤多次給葯,1次給葯消除加快,多次給葯體內積累多。
具體給藥方式:400mg/d1~2次,肌內注射或靜脈滴注(每日1次,靜脈滴注需1h滴畢;每日2次,靜脈滴注需分2次給葯,每次在30min滴畢)。腎功能不良時用藥劑量需要調整(延長給葯時間):中度腎功減退按8mg/Kg/d;嚴重腎功減退按8mg/Kg/2d(肌酐清除率10~19h8mg/Kg/3d/;肌酐清除率6~9h8mg/Kg/4d)。
氨基糖苷類抗生素主要用于敏感需氧革蘭陰性桿菌所致的全身感染。雖然近年來有多種cephalosporins和quinolones藥物在臨床廣泛應用,但由於氨基糖苷類抗生素對銅綠假單胞菌、肺炎桿菌、大腸桿菌等常見革蘭陰性桿菌的PAE較長,所以,仍然被用於治療需氧革蘭陰性桿菌所致的嚴重感染,如腦膜炎、呼吸道、泌尿道、皮膚軟組織、胃腸道、燒傷、創傷及骨關節感染等。
對於敗血症、肺炎、腦膜炎等革蘭陰性桿菌引起的嚴重感染,單獨應用氨基糖苷類抗生素治療時可能療效不佳,此時需聯合應用其他對革蘭陰性桿菌具有強大抗菌活性的抗菌葯,如廣譜半合成penicillins、第三代cephalosporins及quinolones等。
氨基苷類的抗菌作用機制是阻礙細菌蛋白質的合成。作用於細菌蛋白質合成過程,使之合成異常的蛋白,阻礙已合成蛋白的釋放,使細菌細胞膜通透性增加而導致一些重要生理物質外漏,引起細菌死亡。本類藥物對靜止期細菌的殺滅作用較強,是靜止期殺菌劑。其抗菌譜主要是革蘭氏陰性桿菌,包括大腸桿菌、克雷白菌屬、腸桿菌屬、變形桿菌屬、沙雷菌屬、構檬酸桿菌屬等。有的品種對綠膿桿菌或金葡菌,以及結核桿菌等也有抗菌作用。本類抗生素對親瑟菌屬、鏈球菌屬和厭氧菌常無效。
①耳毒性及前庭功能失調:多見於卡那黴素、慶大黴素。耳蝸神經損害,多見於卡那黴素、丁胺卡那黴素。孕婦注射本類藥物可致新生兒聽覺受損,應禁用。
②腎毒性:主要損害近端腎小管曲段,可出現蛋白尿、管型尿、繼而出現紅細胞、尿量減少或增多,進而發生氮質血症、腎功能減退、排鉀增多等。腎毒性大小次序為卡那黴素=西梭黴素>慶大黴素=丁胺卡那黴素>妥布黴素>鏈黴素后神經肌肉阻滯:本類藥物具有類似箭毒阻滯乙酸膽鹼和絡合鈣離子的作用,能引起心肌抑制、呼吸衰竭等,可用新斯的明和鈣劑(靜注)對抗。本類反應以鏈黴素和卡那黴素較多發生,其他品種也不除外。病人原有肌無力症或已接受過肌肉鬆弛葯者更易發生,一般應禁用。
③神經肌肉阻斷作用 各種氨基甙類抗生素均可引起神經肌肉麻痹作用,雖較小見,但有潛在性危險。神經肌肉阻斷作用與劑量及給葯途徑有關,如靜脈滴注速度過快或同時應用肌肉鬆弛劑與全身麻醉藥。重症肌無力者尤易發生,可致呼吸停止。其機制是乙醯膽鹼的釋放需Ca2+的參與,藥物能與突觸前膜上“鈣結合部位”結合,從而阻止乙醯膽鹼釋放。當出現神經肌肉麻痹時,可用鈣劑或新斯的明治療。
④過敏反應,包括過敏性休克、皮疹、蕁麻疹、葯熱、粒細胞減少、溶血性貧血等。不良反應與藥物濃度密切相關,在用藥過程中直進行血葯濃度監測。其他有血象變化、肝臟轉氨酶升高、面部及四肢麻木、周圍神經炎、視力模糊等。口服本類藥物可引起脂肪性腹瀉。菌群失調和二重感染也有發生。