共找到2條詞條名為順鉑的結果 展開
- 兒科用藥
- 順鉑
順鉑
順鉑
順鉑為橙黃色或黃色結晶性粉末。熔點268-272℃(分解)。微溶於水,易溶於二甲基甲醯胺。在水溶液中可逐漸轉化成反式和水解。臨床用於卵巢癌、前列腺癌、睾丸癌、肺癌、鼻咽癌、食道癌、惡性淋巴瘤、頭頸部鱗癌、甲狀腺癌及成骨肉瘤等多種實體腫瘤均能顯示療效。
中文名稱:順鉑
中文別名:順二氯二氨基鉑;順雙氯雙氨絡鉑;順-二氯二氨合鉑;順-雙氯雙氨絡鉑;順氯氨鉑;順-二胺二氯鉑(II);(Z)-二氨二氯鉑;順式-二胺二氯鉑;
英文名稱:cisplatin
英文別名:cis-Dichlorodiammine platinum(II);cis-Dichlorodiamineplatinum(II);cis-Diamminedichloroplatinum(II);cis-Diammineplatinum(II) dichloride;cis-Platinum(II) diammine dichloride;cis-Diamineplatinum(II) dichloride;cis-Diammineplatinum dichloride;Cisplatin;cis-Diammineplatinum(II) dichloride (cis-Dichlorodiammine platinum(II);
CAS號:15663-27-1
MDL號:MFCD00011623
EINECS號:239-733-8
RTECS號:TP2455000
PubChem號:24871609
分子式:ClHNPt
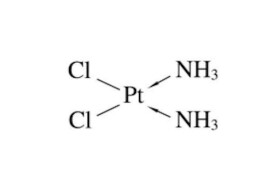
結構式:
![PDD[順鉑]](https://i1.twwiki.net/cover/w200/m8/0/m8018b043205a764834648deceefdfc9e.jpg)
PDD[順鉑]
精確質量:296.94000
PSA:52.04000
LogP:1.59590
外觀與性狀:橙色-黃色至深黃色固體或粉末
密度:3.7
熔點:270ºC
穩定性:Stable. Incompatible with oxidizing agents, aluminium, antioxidants.
儲存條件:Store in a cool, dry, well-ventilated area away from incompatible substances. Poison room locked. Keep containers tightly closed.
符號:GHS05GHS06GHS08
信號詞:危險
危害聲明:H300; H318; H350
警示性聲明:P201; P264; P280; P301 + P310; P305 + P351 + P338; P308 + P313
包裝等級:II
危險類別:6.1(a)
海關編碼:2932999099
危險品運輸編碼:UN 1851/3288
WGK Germany:3
危險類別碼:R45; R25; R41
安全說明:S53-S26-S39-S45
RTECS號:TP2455000
危險品標誌:T
1、疏水參數計算參考值(XlogP):
2、氫鍵供體數量:2
3、氫鍵受體數量:4
4、可旋轉化學鍵數量:0
5、互變異構體數量:
6、拓撲分子極性表面積(TPSA):2
7、重原子數量:5
8、表面電荷:0
9、複雜度:0
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15.共價鍵單元數量:5
由四氯鉑酸鉀與氯化銨、氨水絡合製得。
該品能與DNA結合,引起交叉聯結,從而破壞DNA的功能,並抑制細胞有絲分裂,為一種細胞非特異性藥物。該品抗瘤譜較廣,用於頭頸部鱗癌;卵巢癌;胚胞性癌;精原性細胞瘤;肺癌;甲狀腺癌;淋巴肉瘤及網狀細胞肉瘤等。
S53Avoid exposure - obtain special instructions before use.
避免接觸,使用前須獲得特別指示說明。
S26In case of contact with eyes, rinse immediately with plenty of water and seek medical advice.
不慎與眼睛接觸后,請立即用大量清水沖洗並徵求醫生意見。
S39Wear eye / face protection.
戴護目鏡或面具。
S45In case of accident or if you feel unwell, seek medical advice immediately (show the label whenever possible.)
若發生事故或感不適,立即就醫(可能的話,出示其標籤)。
R45May cause cancer.
可能致癌。
R25Toxic if swallowed.
吞食有毒。
R41Risk of serious damage to the eyes.
對眼睛有嚴重傷害。
本品為(Z)-二氨二氯鉑。按乾燥品計算,含Cl2H6N2Pt應為98.0%~102.0%。
本品為亮黃色至橙黃色的結晶性粉末;無臭。本品在二甲基亞碸中易溶,在二甲基甲醯胺中略溶,在水中微溶,在乙醇中不溶。
(1)取本品約5mg,加硫酸1ml后,即顯灰綠色。
(2)在含量測定項下記錄的色譜圖中,供試品溶液主峰的保留時間應與對照品溶液主峰的保留時間一致。
(3)取本品,加0.9%氯化鈉溶液製成每1ml中約含1mg的溶液,照紫外-可見分光光度法(2010年版藥典二部附錄ⅣA)測定,在301nm的波長處有最大吸收,在247nm的波長處有最小吸收。
(4)本品的紅外光吸收圖譜應與對照的圖譜(《藥品紅外光譜集》297圖)一致。
含鉑量
取本品約0.5g,精密稱定,照熾灼殘渣檢查法(2010年版藥典二部附錄ⅧN,但不加硫酸),在400℃熾灼至恆重,所得殘渣重量即為供試量中含有鉑的重量。按乾燥品計算,含鉑量應為64.6%~65.4%。
含氯量
取本品30mg,精密稱定,照氧瓶燃燒法(2010年版藥典二部附錄ⅦC)進行有機破壞,用氫氧化鈉試液20ml為吸收液,俟燃燒完畢后,強力振搖數分鐘,用少量水沖洗瓶塞及鉑絲,洗液併入吸收液中,加溴酚藍指示液1滴,滴加稀硝酸至溶液變為黃色,再加稀硝酸1ml、乙醇20ml與1%二苯偕肼的乙醇溶液5滴,用硝酸汞滴定液(0.025mol/L)滴定,近終點時強力振搖,繼續滴定至溶液顯淡玫瑰紅色,並將滴定的結果用空白試驗校正。每1ml硝酸汞滴定液(0.025mol/L)相當於1.773mg的氯(Cl),含氯量應為23.0%~24.3%。
溶液的澄清度
取本品20mg,加0.9%氯化鈉溶液20ml溶解后,溶液應澄清。
酸度
取溶液的澄清度項下的溶液,依法測定(2010年版藥典二部附錄ⅥH),pH值應為5.0~7.0。
有關物質
避光操作。取本品,加0.9%氯化鈉溶液溶解並稀釋製成每1ml中約含0.2mg的溶液,作為供試品溶液(臨用新制);精密量取1ml,置50ml量瓶中,用0.9%氯化鈉溶液稀釋至刻度,搖勻,作為對照溶液。照含量測定項下的色譜條件,取對照溶液20μl注入液相色譜儀,調節檢測靈敏度,使主成分色譜峰的峰高約為滿量程的15%。再精密量取供試品溶液和對照溶液各20μl,分別注入液相色譜儀,記錄色譜圖至主成分峰保留時間的2倍。供試品溶液色譜圖中如有雜質峰,相對保留時間約為0.87的雜質峰面積乘以0.569后不得大於對照溶液主峰面積的0.5倍(1.0%),相對保留時間約為1.2的雜質峰面積乘以1.356后不得大於對照溶液的主峰面積(2.0%),其他雜質峰面積的和不得大於對照溶液主峰面積的0.25(0.5%)。
乾燥失重
取本品約0.1g,在105℃乾燥至恆重,減失重量不得過0.5%(2010年版藥典二部附錄Ⅷ L)。
照高效液相色譜法(2010年版藥典二部附錄ⅤD)測定。
色譜條件與系統適用性試驗
用十八烷基硅烷鍵合硅膠為填充劑;以0.003mol/L庚烷磺酸鈉的0.9%氯化鈉溶液為流動相;檢測波長為220nm。理論板數按順鉑峰計算不低於3000,順鉑峰與相鄰雜質峰的分離度應符合要求。
測定法
避光操作。取本品適量,精密稱定,加0.9%氯化鈉溶液溶解並定量稀釋製成每1ml中約含40μg的溶液,精密量取20μl注入液相色譜儀,記錄色譜圖;另取順鉑對照品,同法測定。按外標法以峰面積計算,即得。
順鉑又稱順氯氨鉑、氯氨鉑、DDP、錫鉑、乙鉑定、順-雙氯雙氨絡鉑,是目前常用的金屬鉑類絡合物,在分子中鉑原子對其抗腫瘤作用有重要意義。但只有順式才有意義,反式無效。可與DNA鏈交叉連接,顯示出細胞毒作用。溶解后在體內無需載體轉運,即可通過帶電的細胞膜。由於細胞內氯離子濃度低 (4mmol/L),氯離子為水所取代,電荷呈陽性,具有類似烷化劑雙功能基團的作用,可與細胞核內DNA的鹼基結合,形成三種形式的交聯,造成DNA損傷,破壞DNA複製和轉錄,高濃度時也抑制RNA及蛋白質的合成。順鉑具有抗癌譜廣、乏氧細胞有效、作用性強等優點,已普遍用於治療睾丸癌、卵巢癌、子宮癌、膀胱癌、頸部癌、前列腺癌、腦癌等,療效顯著。但順鉑用於治療癌有一定的毒性,會引起副作用,因此需要不斷尋找毒性較小而臨床效果與順鉑相近的類似物。迄今各國科學家已合成並檢驗了數千種與順鉑相關的金屬配合物,研製出以碳鉑為代表的第二代抗癌鉑配合物。第三代抗癌金屬配合物也已發現,以二氯茂鈦為代表。這些化合物從化學角度上與順鉑無關,但它們對順鉑治療效果不大的某些癌變有較好的效果,且不傷害腎功能。現在這一領域仍在繼續進行大量研究,著重在分子水平上探索金屬配合物抗癌活性的機理。中國已生產商品順鉑和開展這方面的研究工作。
順鉑屬於細胞周期的非特異性藥物,具有細胞毒性,由於癌細胞較正常細胞的增殖和合成更為迅速,癌細胞對本品的細胞毒性作用就更為敏感,可抑制癌細胞DNA複製過程,並損傷其細胞膜上的結構,有較強的廣譜抗癌作用。用於卵巢癌、前列腺癌、睾丸癌等泌尿生殖系統惡性腫瘤,有較好療效。與長春新鹼、環磷醯胺、5-氟尿嘧啶聯用,對惡性淋巴瘤、乳腺癌、頭頸部鱗癌、甲狀腺癌成骨肉瘤等均能顯效。順鉑配合放療治療晚期非小細胞肺癌、鼻咽癌、食管癌等療效突出,對肝癌和軟組織肉瘤也有一定療效。順鉑為強蓄積性藥物,易產生腎毒性,消化道反應較常見,部分患者出現粒細胞減少,但停葯后7~14天內可恢復。
(1)生殖毒性
本品孕婦應用可導致胎兒損害。小鼠實驗中本品表現出致畸性和胚胎毒性。若妊娠期間應用,或給葯期間發現懷孕,應告之患者其對胎兒的潛在危害性。應勸告有生育可能的婦女避免懷孕。有報道在人乳汁中檢測到本品,建議母親應用本品時中止授乳。
(2)遺傳毒性
本品在細胞實驗中表現出致突變性,使組織培養的動物細胞出現染色體畸變。
(3)致癌毒性
進行了BDIX(共50隻)給葯的致癌性實驗,本品腹腔給葯3周,1mg/kg/周,結果首次給葯的455天內,33隻動物死亡,其中13隻死於惡性腫瘤;12隻白血病,1隻為腎肝臟纖維肉瘤。
[體內過程] DDP口服無效,靜脈注射后開始在肝、腎、大小腸及皮膚中分佈最多,18~24小時后腎內積蓄最多,而腦組織中最少。在血漿中消失迅速,呈雙相型。開始血漿半衰期為25~49分鐘,分佈后血漿半衰期為55~73小時。靜脈注射后1小時血漿含量為10%左右,90%與血漿蛋白等大分子結合。排泄較慢,1日內尿中排出19%~34%,4日內尿中僅排出25%~44%,但在全劑量注入后的5日內,僅有27%~43%的順鉑排出體外;膽道或腸道排出甚少,腹腔給葯時腹腔器官的藥物濃度相當於靜脈給葯的2.5~8倍,這對卵巢癌等治療有增效作用。
腎
(2)頭頸部癌:鼻咽癌、甲狀腺癌、喉癌等。
(4)其他:惡性胸腹水;與放療並用,有放射增敏作用。
為治療多種實體瘤的一線用藥。與VP-16聯合(EP方案)為治療SCLC或NSCLC一線方案,聯合MMC、IFO(IMP方案),或NVB等方案為治療NSCLC常用方案,以DDP為主的聯合化療亦為晚期卵巢癌、骨肉瘤及神經母細胞瘤的主要治療方案,與ADM、CTX等聯用對多部位鱗狀上皮癌、移行細胞癌有效,如頭頸部、宮頸、食管及泌尿系腫瘤等。
“PVB”(DDP、VLB、BLM)可治療大部分IV期非精原細胞睾丸癌,緩解率50%~80%。此外,本品為放療增敏劑,國外廣泛用於IV期不能手術的NSCLC的局部放療,可提高療效及改善生存期。
靜脈注射或靜脈滴註:每次20~30mg,或20mg/m2,溶於生理鹽水20~30ml中靜脈注射,或溶於5%葡萄糖注射液250~500ml中靜脈滴注,在第1天和第8天使用為1個周期,一般3~4周重複,可間斷用藥3~4個周期。
大劑量:80~120mg/m2,每3周1次,同時注意水化,使患者尿量保持在2000~3000ml,也可加用甘露醇利尿。
胸腹腔注射:胸腔7~10日1次,每次30~60mg。腹腔每次100~160mg。
動脈注射:每次20~30ml,中由插管推注,連用5日為1周期,間隔3周可重複。動脈灌注主要用於頭頸部腫瘤。
1、腎臟毒性:單次中、大劑量用藥后,偶會出現輕微、可逆的腎功能障礙,可出現微量血尿。多次高劑量和短期內重複用藥,會出現不可逆的腎功能障礙,嚴重時腎小管壞死,導致無尿和尿毒症。
2、消化系統:包括噁心、嘔吐、食慾減低和腹瀉等,反應常在給葯后1~6小時內發生,最長不超過24~48小時。偶見肝功能障礙、血清轉氨酶增加,停葯后可恢復。
3、造血系統:表現為白細胞和(或)血小板的減少,一般與用藥劑量有關,骨髓抑制一般在3周左右達高峰,4~6周恢復。
4、耳毒性:可出現耳鳴和高頻聽力減低,多為可逆性,不須特殊處理。
6、過敏反應:如心率加快,血壓降低、呼吸困難、面部水腫、變態性發熱反應等,都可能出現。
7、其它:
高尿酸血症:常出現腿腫脹和關節痛。
心臟毒性:少見心率失常、心電圖改變、心動過緩或過速、心功能不全等。
免疫系統:會出現免疫抑制反應。
牙齦變化:牙齦會有鉑金屬沉積。
患者接受動脈或靜脈注射的肢體可能出現局部腫脹。疼痛、紅斑及皮膚潰瘍、局部靜脈炎等少見。也有可能出現脫髮、精子、卵子形成障礙和男性乳房女性化等現象。
繼發性非淋巴細胞性白血病的出現與順鉑化療使用有關。
血管性病變,如腦缺血、冠狀動脈缺血、外周血管障礙類似Ravnaud綜合征等副作用少見,但可能與順鉑使用有關。
1、使用
神經
(2)為減輕毒副作用,用藥期間尚應多飲水;用藥前宜選用各類止吐葯;同時備用腎上腺素、皮質激素、抗組織胺葯,以便急救使用;用DDP后可肌肉注射安鈉咖以鞏固療效。
(3)在用藥前、中、后均應監測血、尿及肝腎功能。其停葯指片為:白細胞<3.5x 109/L,血小板<75x 109/L持續性噁心,嘔吐;早期腎臟毒性如尿中白細胞10、紅細胞10、管型5/高倍視野以上者;血清肌酐>186~351mmol/L者;過敏反應;在用藥過程中發現有腎病史、腎功能不良及患有中耳炎的患者。若血清肌酐、尿素氮、白細胞、血小板等恢復到正常水平,一般情況良好,則可重複用藥。
(4)本品可減少BLM的腎排泄而增加其肺毒性;與氨基甙類抗生素合用可發生致命的腎衰,並可能加重耳的損害;抗級別織胺葯、吩噻嗪類等可能會掩蓋DDP的耳毒性。
(5)DDP在生理鹽水中溶解較慢,可加溫30℃左右振蕩助溶,也可選用溶液製劑。
2、下列患者用藥特別慎重:
即往有腎病史、造血系統功能不全、聽神經功能障礙、用藥前曾接受其它化療或放射治療、及非順鉑引起的外周神經炎等。
3、治療前後,治療期間和每一療程之前,應作如下檢查:肝、腎功能、全血計數、血鈣以及聽神經功能、神經系統功能等檢查。此外,在治療期間,每周應檢查全血計數。通常需待器官功能恢復正常后,才可重複下一療程。
4、化療期間與化療后,男女病人均需嚴格避孕。治療后若想懷孕,需事先進行遺傳學諮詢。
5、順鉑可能影響注意力集中、駕駛和機械操作能力。
6、本品應避免接觸鋁金屬(如鋁金屬注射針器等)。
7、在化療期間與化療后,病人必需飲用足夠的水份。
本品孕婦應用可導致胎兒損害,有報道在人乳汁中檢測到本品,故建議哺乳期婦女應用本品時中止授乳。孕婦禁用。
(2)抗組胺葯、酚噻嗪類葯或噻噸類葯(thioxanthene)與順鉑合用,可能掩蓋耳毒性的癥狀,如耳鳴、眩暈等。
(3)順鉑誘發的腎功能損害可導致博來黴素(甚至小劑量)的毒性反應。
(4)與各種骨髓抑製劑或放射治療同用,可增加毒性作用,用量應減少。
(5)青黴胺或其它的蝥合劑、會減弱順鉑的活性。故本品不應與蝥合劑同時應用。
(6)與異環磷醯胺合用,會加重蛋白尿,同時有可能會增加耳毒性。
禁用諸如速尿等利尿劑以增加尿量。
(8)病人接受順鉑化療后至少三個月,才可接受病毒疫苗接種。
注射劑:10mg/支,20mg/支,30mg/支,50mg/支。
藥物劑量超過120mg/m2,其毒性增加,尤其是腎毒性、骨髓毒性。
遮光,密閉室溫保存。
| 文獻、期刊報道的毒性作用試驗數據 | |||||
|---|---|---|---|---|---|
| 編號 | 毒性類型 | 測試方法 | 測試對象 | 使用劑量 | 毒性作用 |
| 1 | 急性毒性 | 靜脈注射 | 成年男性 | 2140 ug/kg/5D-I | 1.腎、輸尿管和膀胱毒性——腎小管發生變化 (包括急性腎功能衰竭,急性腎小管壞死) |
| 2 | 急性毒性 | 靜脈注射 | 人類 | 1500 ug/kg/6D-I | 1.耳毒性——視力變化 2.腎、輸尿管和膀胱毒性——腎功能下降 3.血液毒性——骨髓發生變化 |
| 3 | 急性毒性 | 靜脈注射 | 人類 | 500 ug/kg/13D-I | 1.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) 2.腎、輸尿管和膀胱毒性——腎功能下降 3.血液毒性——其他變化 |
| 4 | 急性毒性 | 靜脈注射 | 人類 | 2500 ug/kg | 1.行為毒性——出現幻覺,感知扭曲 2.胃腸道毒性——噁心、嘔吐 3.腎、輸尿管和膀胱毒性——腎功能下降 |
| 5 | 急性毒性 | 靜脈注射 | 人類 | 72 mg/kg/25D-I | 1.胃腸道毒性——噁心、嘔吐 |
| 6 | 急性毒性 | Intradermal | 人類 | 40 ng/kg | 1.皮膚和附件毒性——對皮膚有刺激性(局部暴露后) 2.皮膚和附件毒性——皮膚腐蝕(局部暴露后) |
| 7 | 急性毒性 | 腸外 | 成年男性 | 2140 ug/kg/5D-I | 1.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) |
| 8 | 急性毒性 | 未報告 | 兒童 | 19200 ug/kg/12W-I | 1.耳毒性——視力變化 |
| 9 | 急性毒性 | 口服 | 大鼠 | 25800 ug/kg | 1.行為毒性——運動行為發生變化(具體情況具體分析) 2.胃腸道毒性——運動過度、腹瀉 3.血液毒性——正細胞性貧血 |
| 10 | 急性毒性 | 腹腔注射 | 大鼠 | 6400 ug/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 11 | 急性毒性 | 皮下注射 | 大鼠 | 8100 ug/kg | 1.肺部、胸部或者呼吸毒性——紫紺 2.胃腸道毒性——運動過度、腹瀉 3.腎、輸尿管和膀胱毒性——尿量增加 |
| 12 | 急性毒性 | 靜脈注射 | 大鼠 | 8 mg/kg | 1.腎、輸尿管和膀胱毒性——其他變化 |
| 13 | 急性毒性 | 肌肉注射 | 大鼠 | 9200 ug/kg | 1.行為毒性——運動行為發生變化(具體情況具體分析) 2.胃腸道毒性——運動過度、腹瀉 3.血液毒性——正細胞性貧血 |
| 14 | 急性毒性 | 未報告 | 大鼠 | >5 mg/kg | 1.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) |
| 15 | 急性毒性 | 口服 | 小鼠 | 32700 ug/kg | 1.肺部、胸部或者呼吸毒性——紫紺 2.胃腸道毒性——運動過度、腹瀉 3.腎、輸尿管和膀胱毒性——尿量增加 |
| 16 | 急性毒性 | 腹腔注射 | 小鼠 | 6600 ug/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 17 | 急性毒性 | 皮下注射 | 小鼠 | 13 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 18 | 急性毒性 | 靜脈注射 | 小鼠 | 11 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 19 | 急性毒性 | 肌肉注射 | 小鼠 | 17900 ug/kg | 1.行為毒性——運動行為發生變化(具體情況具體分析) 2.胃腸道毒性——運動過度、腹瀉 3.血液毒性——正細胞性貧血 |
| 20 | 急性毒性 | 腸外 | 小鼠 | 22 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 21 | 急性毒性 | 未報告 | 小鼠 | 10900 ug/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 22 | 急性毒性 | 靜脈注射 | 狗 | 2500 ug/kg | 1.胃腸道毒性——其他變化 2.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) 3.血液毒性——出現高鐵血紅蛋白、碳氧血紅蛋白 |
| 23 | 急性毒性 | 靜脈注射 | 猴 | 250 ug/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 24 | 急性毒性 | 腹腔注射 | 豚鼠 | 9700 ug/kg | 1.耳毒性——視力變化 |
| 25 | 急性毒性 | 腸外 | 青蛙 | 17 mg/kg | 1.行為毒性——驚厥或癲癇發作閾值受到影響 2.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) |
| 26 | 急性毒性 | 靜脈注射 | 哺乳動物 | 8 mg/kg | 1.胃腸道毒性——噁心、嘔吐 |
| 27 | 慢性毒性 | 腹腔注射 | 大鼠 | 24 mg/kg/3D-I | 1.肝毒性——其他變化 2.腎、輸尿管和膀胱毒性——其他變化 3.營養和代謝系統毒性——金屬離子濃度發生變化 |
| 28 | 慢性毒性 | 腹腔注射 | 大鼠 | 9 mg/kg/5D-I | 1.胃腸道毒性——其他變化 2.生化毒性——抑制或誘導其他酶 |
| 29 | 慢性毒性 | 腹腔注射 | 大鼠 | 22680 ug/kg/35D-C | 1.腎、輸尿管和膀胱毒性——膀胱重量發生變化 2.內分泌毒性——胸腺重量變化 3.血液毒性——正細胞性貧血 |
| 30 | 慢性毒性 | 腹腔注射 | 大鼠 | 23296 ug/kg/26W-C | 1.肝毒性——肝重量發生變化 2.腎、輸尿管和膀胱毒性——尿中成分發生變化 3.內分泌毒性——胸腺重量變化 |
| 31 | 慢性毒性 | 腹腔注射 | 大鼠 | 14 mg/kg/7D-I | 1.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) 2.營養和代謝系統毒性——體重下降或體重增加速率下降 3.慢性病相關毒性——死亡 |
| 32 | 慢性毒性 | 腹腔注射 | 大鼠 | 18 mg/kg/5W-I | 1.周圍神經毒性——神經或神經鞘結構發生變化 2.慢性病相關毒性——死亡 |
| 33 | 慢性毒性 | 靜脈注射 | 大鼠 | 16200 ug/kg/26W-I | 1.心臟毒性——其他變化 2.腎、輸尿管和膀胱毒性——其他變化 3.內分泌毒性——其他變化 |
| 34 | 慢性毒性 | 腹腔注射 | 大鼠 | 18 mg/kg/9W-I | 1.周圍神經毒性——神經或神經鞘結構發生變化 |
| 35 | 慢性毒性 | 腹腔注射 | 大鼠 | 22800 ug/kg/6W-I | 1.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) 2.血液毒性——骨髓發生變化 3.骨骼肌毒性——其他變化 |
| 36 | 慢性毒性 | 靜脈注射 | 大鼠 | 22 mg/kg/4W-I | 1.血液毒性——血清成分發生變化(如TP、膽紅素、膽固醇) 2.血液毒性——白細胞計數發生變化 3.血液毒性——血小板計數發生變化 |
| 37 | 慢性毒性 | 靜脈注射 | 大鼠 | 18 mg/kg/20D-I | 1.腎、輸尿管和膀胱毒性——其他變化 2.血液毒性——血清成分發生變化(如TP、膽紅素、膽固醇) 3.生化毒性——抑制或誘導過氧化氫酶 |
| 38 | 慢性毒性 | 腹腔注射 | 小鼠 | 40 mg/kg/8W-I | 1.周圍神經毒性——三叉神經感官發生變化 2.營養和代謝系統毒性——體重下降或體重增加速率下降 3.慢性病相關毒性——死亡 |
| 39 | 慢性毒性 | 靜脈注射 | 小鼠 | 11 mg/kg/5D-I | 1.大腦毒性——腦重量發生變化 2.腎、輸尿管和膀胱毒性——膀胱重量發生變化 3.營養和代謝系統毒性——體重下降或體重增加速率下降 |
| 40 | 慢性毒性 | 靜脈注射 | 狗 | 10500 ug/kg/90D | 1.血液毒性——血小板減少 2.營養和代謝系統毒性——體重下降或體重增加速率下降 3.生化毒性——抑制或誘導磷酸酶 |
| 41 | 慢性毒性 | 靜脈注射 | 狗 | 10800 ug/kg/26W-I | 1.腎、輸尿管和膀胱毒性——膀胱重量發生變化 2.血液毒性——血小板計數發生變化 3.慢性病相關毒性——睾丸重量發生變化 |
| 42 | 慢性毒性 | 靜脈注射 | 狗 | 3750 ug/kg/5D-I | 1.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) 2.血液毒性——骨髓發生變化 3.慢性病相關毒性——死亡 |
| 43 | 慢性毒性 | 靜脈注射 | 猴 | 12500 ug/kg/5D-I | 1.胃腸道毒性——其他變化 2.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) 3.血液毒性——骨髓發生變化 |
| 44 | 慢性毒性 | 靜脈注射 | 猴 | 12500 ug/kg/12W-I | 1.周圍神經毒性——神經或神經鞘結構發生變化 2.胃腸道毒性——噁心、嘔吐 3.腎、輸尿管和膀胱毒性——腎小管發生變化(包括急性腎功能衰竭,急性腎小管壞死) |
| 45 | 慢性毒性 | 腹腔注射 | 豚鼠 | 7500 ug/kg/15D-I | 1.耳毒性——視力變化 2.耳毒性——耳蝸結構或功能發生變化 3.慢性病相關毒性——死亡 |
| 46 | 慢性毒性 | 腹腔注射 | 豚鼠 | 18 mg/kg/9D-I | 1.血液毒性——血清成分發生變化(如TP、膽紅素、膽固醇) 2.營養和代謝系統毒性——體重下降或體重增加速率下降 3.慢性病相關毒性——死亡 |
| 47 | 慢性毒性 | 腹腔注射 | 豚鼠 | 15 mg/kg/30D-I | 1.耳毒性——耳蝸結構或功能發生變化 |
| 48 | 突變毒性 | 鼠傷寒沙門氏菌 | 250 ng/plate | ||
| 49 | 突變毒性 | 鼠傷寒沙門氏菌 | 300 ng/plate | ||
| 50 | 突變毒性 | 鼠傷寒沙門氏菌 | 1 nmol/plate | ||
| 51 | 突變毒性 | 鼠傷寒沙門氏菌 | 10 mg/L/20H (持續) | ||
| 52 | 突變毒性 | 大腸埃希氏菌 | 25 ug/plate | ||
| 53 | 突變毒性 | 大腸埃希氏菌 | 3 mg/L | ||
| 54 | 突變毒性 | 大腸埃希氏菌 | 50 umol/L | ||
| 55 | 突變毒性 | 大腸埃希氏菌 | 125 ng/plate | ||
| 56 | 突變毒性 | 大腸埃希氏菌 | 50 umol/L | ||
| 57 | 突變毒性 | 大腸埃希氏菌 | 35 mg/L | ||
| 58 | 突變毒性 | 大腸埃希氏菌 | 26600 nmol/L | ||
| 59 | 突變毒性 | 大腸埃希氏菌 | 250 umol/L | ||
| 60 | 突變毒性 | 大腸埃希氏菌 | 1 ug/plate | ||
| 61 | 突變毒性 | 枯草芽孢桿菌 | 15 umol/L/3H (持續) | ||
| 62 | 突變毒性 | 枯草芽孢桿菌 | 1 ug/plate | ||
| 63 | 突變毒性 | 微生物 | 250 mg/L | ||
| 64 | 突變毒性 | 微生物 | 1 mmol/L | ||
| 65 | 突變毒性 | 微生物 | 60 nmol/L | ||
| 66 | 突變毒性 | 微生物 | 1 mmol/L | ||
| 67 | 突變毒性 | 口服 | 果蠅 | 10 umol/L | |
| 68 | 突變毒性 | 腸外 | 果蠅 | 200 umol/L | |
| 69 | 突變毒性 | 腸外 | 果蠅 | 830 umol/L | |
| 70 | 突變毒性 | 口服 | 果蠅 | 40 ppm | |
| 71 | 突變毒性 | 腸外 | 果蠅 | 200 umol/L | |
| 72 | 突變毒性 | 粗糙脈孢菌 | 200 umol/L | ||
| 73 | 突變毒性 | 釀酒酵母 | 50 mg/L | ||
| 74 | 突變毒性 | 釀酒酵母 | 50 mg/L | ||
| 75 | 突變毒性 | 鮭魚精子 | 10 mg/L | ||
| 76 | 突變毒性 | 人類淋巴細胞 | 8250 nmol/L | ||
| 77 | 突變毒性 | 人類白細胞 | 500 ug/L | ||
| 78 | 突變毒性 | 人類成纖維細胞 | 5 umol/L | ||
| 79 | 突變毒性 | 人類白細胞 | 100 umol/L | ||
| 80 | 突變毒性 | 人類卵巢 | 20 umol/L | ||
| 81 | 突變毒性 | 人類 細胞 | 10 umol/L | ||
| 82 | 突變毒性 | 人類卵巢 | 40 umol/L | ||
| 83 | 突變毒性 | 人類卵巢 | 10 umol/L | ||
| 84 | 突變毒性 | 人類 細胞 | 5 mg/L | ||
| 85 | 突變毒性 | 人類成纖維細胞 | 20 umol/L | ||
| 86 | 突變毒性 | 人類 細胞 | 10 umol/L | ||
| 87 | 突變毒性 | 人類 細胞 | 45 umol/L | ||
| 88 | 突變毒性 | 人類淋巴細胞 | 12 umol/L | ||
| 89 | 突變毒性 | 海拉細胞 | 5 umol/L | ||
| 90 | 突變毒性 | 海拉細胞 | 5 umol/L | ||
| 91 | 突變毒性 | 人類非 | 10 umol/L | ||
| 92 | 突變毒性 | 人類 細胞 | 10 umol/L | ||
| 93 | 突變毒性 | 人類 細胞 | 10 umol/L | ||
| 94 | 突變毒性 | 人類 細胞 | 10 umol/L | ||
| 95 | 突變毒性 | 人類成纖維細胞 | 10 umol/L | ||
| 96 | 突變毒性 | 海拉細胞 | 500 nmol/L | ||
| 97 | 突變毒性 | 人類淋巴細胞 | 10 mg/L | ||
| 98 | 突變毒性 | 人類 細胞 | 5 umol/L | ||
| 99 | 突變毒性 | 人類 細胞 | 5 umol/L | ||
| 100 | 突變毒性 | 人類淋巴細胞 | 8250 nmol/L | ||
| 101 | 突變毒性 | 人類卵巢 | 5 umol/L | ||
| 102 | 突變毒性 | 人類 細胞 | 20 umol/L | ||
| 103 | 突變毒性 | 人類鼠傷寒沙門氏菌 | 24 mg/kg | ||
| 104 | 突變毒性 | 人類 細胞 | 10 umol/L | ||
| 105 | 突變毒性 | 人類淋巴細胞 | 1 mg/L/24H | ||
| 106 | 突變毒性 | 人類 細胞 | 50 mg/L | ||
| 107 | 突變毒性 | 人類 細胞 | 3300 nmol/L | ||
| 108 | 突變毒性 | 人類淋巴細胞 | 250 ng/L/96H | ||
| 109 | 突變毒性 | 腹腔注射 | 大鼠 | 3500 ug/kg | |
| 110 | 突變毒性 | 大鼠 細胞 | 10 umol/L | ||
| 111 | 突變毒性 | 靜脈注射 | 大鼠 | 8 mg/kg | |
| 112 | 突變毒性 | 腹腔注射 | 大鼠 | 5 mg/kg | |
| 113 | 突變毒性 | 腹腔注射 | 大鼠 | 4 mg/kg | |
| 114 | 突變毒性 | 靜脈注射 | 大鼠 | 8500 ug/kg | |
| 115 | 突變毒性 | 大鼠腎 | 10 umol/L | ||
| 116 | 突變毒性 | 大鼠、鼠傷寒沙門氏菌 | 40 mg/kg | ||
| 117 | 突變毒性 | 腹腔注射 | 大鼠 | 650 ug/kg/5D | |
| 118 | 突變毒性 | 大鼠 細胞 | 1 umol/L | ||
| 119 | 突變毒性 | 腹腔注射 | 小鼠 | 100 ug/kg | |
| 120 | 突變毒性 | 小鼠 細胞 | 62500 ng/L | ||
| 121 | 突變毒性 | 腹腔注射 | 小鼠 | 10 mg/kg | |
| 122 | 突變毒性 | 小鼠白細胞 | 4 mg/L | ||
| 123 | 突變毒性 | 靜脈注射 | 小鼠 | 20 mg/kg | |
| 124 | 突變毒性 | 小鼠 細胞 | 1 mg/L | ||
| 125 | 突變毒性 | 小鼠 細胞 | 1 mg/L | ||
| 126 | 突變毒性 | 小鼠乳腺 | 5 mg/L | ||
| 127 | 突變毒性 | 小鼠腹水瘤細胞 | 100 umol/L | ||
| 128 | 突變毒性 | 小鼠腹水瘤細胞 | 100 umol/L | ||
| 129 | 突變毒性 | 小鼠淋巴細胞 | 50 mg/L | ||
| 130 | 突變毒性 | 小鼠白細胞 | 1 mg/L | ||
| 131 | 突變毒性 | 小鼠 細胞 | 500 ug/L | ||
| 132 | 突變毒性 | 腹腔注射 | 小鼠 | 12 mg/kg | |
| 133 | 突變毒性 | 小鼠鼠傷寒沙門氏菌 | 2500 ug/kg | ||
| 134 | 突變毒性 | 腹腔注射 | 小鼠 | 500 ug/kg | |
| 135 | 突變毒性 | 小鼠 細胞 | 8 mg/kg | ||
| 136 | 突變毒性 | 小鼠白細胞 | 5 mg/L | ||
| 137 | 突變毒性 | 小鼠 細胞 | 2 mg/L | ||
| 138 | 突變毒性 | 靜脈注射 | 小鼠 | 1300 ug/kg | |
| 139 | 突變毒性 | 小鼠 細胞 | 4 umol/L | ||
| 140 | 突變毒性 | 小鼠胚胎 | 100 nmol/L | ||
| 141 | 突變毒性 | 腹腔注射 | 小鼠 | 2500 ug/kg | |
| 142 | 突變毒性 | 小鼠大腸埃希氏菌 | 10 mg/L | ||
| 143 | 突變毒性 | 小鼠腹水瘤細胞 | 18200 ug/kg | ||
| 144 | 突變毒性 | 腹腔注射 | 小鼠 | 10 mg/kg | |
| 145 | 突變毒性 | 靜脈注射 | 小鼠 | 10 mg/kg | |
| 146 | 突變毒性 | 腹腔注射 | 倉鼠 | 1 mg/kg | |
| 147 | 突變毒性 | 倉鼠肺 | 680 nmol/L | ||
| 148 | 突變毒性 | 倉鼠卵巢 | 5 mg/L | ||
| 149 | 突變毒性 | 倉鼠腎 | 1 umol/L | ||
| 150 | 突變毒性 | 倉鼠胚胎 | 100 nmol/L | ||
| 151 | 突變毒性 | 倉鼠卵巢 | 50 umol/L | ||
| 152 | 突變毒性 | 倉鼠肺 | 11 umol/L/2H | ||
| 153 | 突變毒性 | 倉鼠卵巢 | 1 umol/L | ||
| 154 | 突變毒性 | 倉鼠 細胞 | 1 mmol/L | ||
| 155 | 突變毒性 | 倉鼠肺 | 30 umol/L | ||
| 156 | 突變毒性 | 倉鼠卵巢 | 5 mg/L | ||
| 157 | 突變毒性 | 倉鼠卵巢 | 5 mg/L | ||
| 158 | 突變毒性 | 倉鼠肺 | 680 nmol/L | ||
| 159 | 突變毒性 | 倉鼠卵巢 | 5 mg/L | ||
| 160 | 突變毒性 | 倉鼠 細胞 | 330 nmol/L | ||
| 161 | 突變毒性 | 倉鼠肺 | 1 ng/L/2H | ||
| 162 | 突變毒性 | 倉鼠胚胎 | 100 nmol/L | ||
| 163 | 突變毒性 | 倉鼠卵巢 | 200 ug/L | ||
| 164 | 突變毒性 | 腹腔注射 | 倉鼠 | 10 mg/kg | |
| 165 | 突變毒性 | 倉鼠卵巢 | 1 umol/L | ||
| 166 | 突變毒性 | 倉鼠肺 | 2 mg/L/2H | ||
| 167 | 突變毒性 | 哺乳動物淋巴細胞 | 100 umol/L | ||
| 168 | 突變毒性 | 兔腎 | 5 mg/L/24H | ||
| 169 | 突變毒性 | 兔腎 | 5 mg/L/24H | ||
| 170 | 突變毒性 | 靜脈注射 | 兔 | 1250 ug/kg | |
| 171 | 突變毒性 | 兔淋巴細胞 | 100 ug/L | ||
| 172 | 致癌性 | 腹腔注射 | 小鼠 | 7500 ug/kg | 1.致癌性——腫瘤(根據RTECS標準) 2.皮膚和附件毒性——腫瘤 3.生殖毒性——胎盤腫瘤 |
| 173 | 致癌性 | 腹腔注射 | 小鼠 | 16 mg/kg/19W-I | 1.致癌性——致癌(根據RTECS標準) 2.肺部、胸部或者呼吸毒性——腫瘤 |
| 174 | 致癌性 | 腹腔注射 | 小鼠 | 16204 ug/kg/10W-I | 1.致癌性——腫瘤(根據RTECS標準) 2.肺部、胸部或者呼吸毒性——腫瘤 |
| 175 | 致癌性 | 腹腔注射 | 小鼠 | 32408 ug/kg/10W-I | 1.致癌性——腫瘤(根據RTECS標準) 2.肺部、胸部或者呼吸毒性——腫瘤 |
| 176 | 生殖毒性 | 腹腔注射 | 大鼠 | 4500 ug/kg,雌性受孕 17-22 天后 | 1.生殖毒性——影響新生兒活力指數(如在出生第4天還活著) |
| 177 | 生殖毒性 | 腹腔注射 | 大鼠 | 2750 ug/kg,雌性受孕 7-11 天后 | 1.生殖毒性——產生額外的胚胎結構(如胎盤、臍帶) 2.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) 3.生殖毒性——影響新生兒活產指數 |
| 178 | 生殖毒性 | 腹腔注射 | 大鼠 | 9 mg/kg,雄性配種 3 天前 | 1.生殖毒性——睾丸,附睾,輸精管發生變化 |
| 179 | 生殖毒性 | 腹腔注射 | 大鼠 | 300 ug/kg,雌性受孕 6 天后 | 1.生殖毒性——肌肉骨骼系統發育異常 |
| 180 | 生殖毒性 | 腹腔注射 | 大鼠 | 13 mg/kg,雌性受孕 17-22 天后 | 1.生殖毒性——影響新生兒的行為 2.生殖毒性——新生兒身體變化 |
| 181 | 生殖毒性 | 腹腔注射 | 大鼠 | 3 mg/kg,雌性受孕 3 天后 | 1.生殖毒性——植入后死亡率增加 |
| 182 | 生殖毒性 | 皮下注射 | 大鼠 | 10 mg/kg,雄性配種 5 天前 | 1.生殖毒性——雄性生精功能異常(包括遺傳物質,精子形態,精子活力和計數) 2.生殖毒性——睾丸,附睾,輸精管發生變化 3.生殖毒性——前列腺,精囊,考伯氏腺,附屬腺體發生變化 |
| 183 | 生殖毒性 | 皮下注射 | 大鼠 | 10 mg/kg,雄性配種 5 天前 | 1.生殖毒性——雄性生精功能異常(包括遺傳物質,精子形態,精子活力和計數) 2.生殖毒性——睾丸,附睾,輸精管發生變化 3.生殖毒性——前列腺,精囊,考伯氏腺,附屬腺體發生變化 |
| 184 | 生殖毒性 | 靜脈注射 | 大鼠 | 4125 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——胚胎或胎兒死亡 2.生殖毒性——新生兒死胎 3.生殖毒性——影響新生兒活力指數(如在出生第4天還活著) |
| 185 | 生殖毒性 | 靜脈注射 | 大鼠 | 660 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——產生額外的胚胎結構(如胎盤、臍帶) 2.生殖毒性——肌肉骨骼系統發育異常 3.生殖毒性——影響新生兒的行為 |
| 186 | 生殖毒性 | 靜脈注射 | 大鼠 | 1650 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) 2.生殖毒性——其他變化 |
| 187 | 生殖毒性 | 靜脈注射 | 大鼠 | 4125 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——新生兒體重增加量減少 2.生殖毒性——新生兒身體變化 |
| 188 | 生殖毒性 | 未報告 | 大鼠 | 1 mg/kg,多代 | 1.生殖毒性——影響新生兒的行為 |
| 189 | 生殖毒性 | 口服 | 小鼠 | 8 mg/kg,雌性受孕 12 天后 | 1.生殖毒性——中樞神經系統發育異常 |
| 190 | 生殖毒性 | 腹腔注射 | 小鼠 | 8 mg/kg,雌性受孕 12 天后 | 1.生殖毒性——中樞神經系統發育異常 |
| 191 | 生殖毒性 | 腹腔注射 | 小鼠 | 3 mg/kg,雌性受孕 8 天后 | 1.生殖毒性——植入后死亡率增加 2.生殖毒性——影響產仔數 3.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) |
| 192 | 生殖毒性 | 腹腔注射 | 小鼠 | 1100 ug/kg,雄性配種 1 天前 | 1.生殖毒性——雄性生精功能異常(包括遺傳物質,精子形態,精子活力和計數) |
| 193 | 生殖毒性 | 腹腔注射 | 小鼠 | 20 mg/kg,雌性受孕 13 天后 | 1.生殖毒性——影響胎兒或胚胎細胞遺傳物質 2.生殖毒性——中樞神經系統發育異常 |
| 194 | 生殖毒性 | 腹腔注射 | 小鼠 | 300 ug/kg,雌性受孕 8 天后 | 1.生殖毒性——胎兒毒性(如胎兒發育不良,但不至死亡) |
| 195 | 生殖毒性 | 皮下注射 | 小鼠 | 350 mg/kg,雄性配種 5 周前 | 1.生殖毒性——雄性生精功能異常(包括遺傳物質,精子形態,精子活力和計數) 2.生殖毒性——睾丸,附睾,輸精管發生變化 |
| 196 | 生殖毒性 | 靜脈注射 | 小鼠 | 1100 ug/kg,雄性配種 1 天前 | 1.生殖毒性——雄性生精功能異常(包括遺傳物質,精子形態,精子活力和計數) |
| 197 | 生殖毒性 | 靜脈注射 | 兔 | 1625 ug/kg,雌性受孕 6-18 天后 | 1.生殖毒性——影響產仔數 2.生殖毒性——胚胎或胎兒死亡 |