腸毒素
引起葡萄球菌食物中毒的致病物質
腸毒素是一種外毒素,通常指金黃色葡萄球菌產生的一種相對熱穩定的毒素。根據抗原性分為A-E,G-I8個血清型。腸毒素是蛋白質,溶於水,相對分子質量約為30000,耐熱(目前有一種大腸桿菌不耐熱腸毒素新興突變體),食品中的毒素不因加工而滅活;對蛋白酶與有耐性,故在消化道中不易被破壞。食入腸毒素可引起劇烈嘔吐和腹瀉,是葡萄球菌性食物中毒的主要致病因子。腸毒素有時也指專對腸粘膜細胞具有特殊毒性作用的毒素。腸組織產生的毒素。
腹瀉是全球範圍內引起5歲以下幼童死亡的第二大病因,而產腸毒素大腸桿菌(ETEC)是引起腹瀉的最常見病原菌,其產生的細菌定植因子(CFs)和腸毒素是關鍵的毒力因子。CFs介導細菌黏附宿主小腸上皮細胞並完成定植,產生熱敏腸毒素(LT)和熱穩定腸毒素(ST)破壞宿主上皮細胞內的體液平衡,使體液和電介質過量分泌從而導致腹瀉。預防ETEC腹瀉的首選方法是使用能激發宿主產生抗黏附素免疫力和抗腸毒素免疫力的疫苗,阻斷ETEC黏附和定植並中和腸毒素。目前一種名為Dukoral®的霍亂疫苗因能刺激機體產生抗熱敏毒素免疫,已經被一些國家批准用於短期保護和預防旅行者腹瀉。
人源ETEC是一類可分泌LT和/或STa的大腸桿菌,大部分菌株還會產生一個或多個CFs。CFs主要是菌毛狀或纖絲狀的生物多聚纖絲,每個菌體表面存在數百個這樣的重複結構單元。目前,至少有25種不同的CFs被證明與腹瀉相關,其中7種常見於嚴重腹瀉病例。這些CFs介導細菌黏附到宿主上皮細胞並定植於小腸,隨後在小腸上皮細胞近端產生和釋放LT和STa腸毒素,刺激體液過量分泌,引起腹瀉。
LT是典型的A:B型全毒素,包含1個A亞單位和5個B亞單位,和霍亂弧菌產生的霍亂毒素極其相近。LT-B亞單位可以結合到上皮細胞單唾液酸四己糖神經節苷脂之類的神經節苷脂受體上,繼而釋放A亞單位激活腺苷酸環化酶途徑,導致宿主細胞內cAMP水平上升,激活cAMP依賴的蛋白激酶,引起氯化物的過量分泌,同時抑制氯化鈉的吸收,最終導致體液的過量分泌。僅含19個氨基酸的腸毒素STa通過和宿主腸上皮細胞外膜上的鳥苷酸環化酶C跨膜受體結合,激活鳥苷酸環化酶途徑,導致細胞內cGMP水平上升。和cAMP水平上升的效應類似,cGMP水平的上升促進了宿主腸上皮細胞氯化物的分泌,同時抑制了氯化鈉的吸收,從而導致了體液的過量分泌。當體液的分泌量遠遠超出腸腔的重吸收能力時,引起水樣腹瀉,同時,由於體液大量丟失可導致脫水和電解質失衡,若得不到及時的治療,嚴重者可導致急性死亡。對ETEC腹瀉患者的流行病學調研發現,呈地方性流行的地區以嬰兒和小於3歲的兒童感染最為常見,且發病率隨年齡增長而降低。而遊客的發病率與在流行地區的滯留時間長短有關,與年齡變化趨勢無關。這表明人自然接觸病原后確實能產生抵抗ETEC感染的免疫力,這種後天獲得的免疫力能夠保護人體抵抗感染。
列。這些毒素引起毒素休克綜合征、食物中毒和幾種過敏性疾病、自身免疫性疾病。SEs是一組血清學上互不相同的熱穩定腸毒素,它的功能既包括作為潛在的胃腸道毒素也包括作為超抗原刺激非特異性T細胞的增殖。儘管這兩種獨立的功能作用在蛋白質的不同區域,但這些作用之間仍然有著很高的相關性,並且在絕大多數的例子中
大多數的超抗原作用(由於基因突變)又引起多數腸毒素作用。
金黃色葡萄球菌
該菌產生的主要毒素有:腸毒素(Staphylococcal enterotoxins,SE)、葡萄球菌溶素、表皮剝脫毒素、殺白細胞素、毒性休克綜合征毒素—1等;產生的主要酶類有:凝固酶、耐熱核酸酶、葡激酶等,其中腸毒素在該菌的致病性中起著重要的作用。
葡萄球菌的致病力取決於它所產生的毒素和酶的能力,致病性菌株可產生腸毒素、溶血毒素、殺白細胞素、血漿凝固酶、耐熱DNA酶等。其中腸毒素、血漿凝固酶和耐熱DNA酶有密切關係,能產生腸毒素的葡萄球菌在厭氧條件下發酵葡萄糖,可產生耐熱的核酸內切酶。
除了金黃色葡萄球菌,可產生腸毒素的細菌還包括:大腸桿菌、產氣莢膜菌、艱難梭菌、脆弱類桿菌等。沙門氏菌部分菌型也可產生。
1、腸毒素是一組具有超抗原活性的細菌毒素,易溶於水和鹽溶液,分子量為26~30kDa,對熱穩定,可耐受100℃煮沸30min不被破壞,仍有致病性,能抵抗胃腸液中蛋白酶的水解作用,故在消化道中不斷被破壞。
2、可引起猴、貓嘔吐,可能是毒素作用於腸道神經受體后,刺激嘔吐中樞所致。
依據腸毒素(SE)抗原性和等電點的不同,發現SE有A、B、C、D、E、F、G、H、I和J等10個毒素血清型,以A和D型最常見,其中以A型的毒力最強,攝入1μg即能引起中毒,所以是引起食物中毒最多的,而C型又可分為C1、C2和C3三個亞型,所有的SE都是由單個無分支的多肽鏈所組成,易溶於水和鹽溶液。一株金黃色葡萄球菌能產生一型或兩型以上的腸毒素;但是,在產混合型毒素菌株中又常以某一型的腸毒素為主,因此,腸毒素的型別不能代表細菌的型別。
腸毒素性食物中毒
據美國疾病預防控制中心報告,由金黃色葡萄球菌引起的食物中毒僅次於大腸埃希菌,居第二位,占細菌性食物中毒的33%,加拿大的發生率更高,占細菌性食物中毒的45%,中國每年發生的此類中毒事件也非常多,全國各地均有報告,是疾病預防控制部門重點監測的疾病。
一般情況下是患者進食了被金黃色葡萄球菌產生的腸毒素(一般認為約1μg/kg)刺激患者嘔吐中樞而導致以嘔吐為主要癥狀的食物中毒。中毒食品多為奶、肉、魚、蛋及其製品以及剩飯、剩菜和冷盤,所以,應將食品,尤其是含蛋白質多、水分多、澱粉多的熟食儲存於4℃環境中,以防止微生物大量繁殖,繼而產生大量的毒素。
研究顯示金黃色葡萄球菌的腸毒素不僅可引起食物中毒,在該菌引起的化膿性感染中也起重要作用。研究人員在進行燙傷膿毒血症大鼠急性肺損傷研究時,發現金黃色葡萄球菌腸毒素B型的單克隆抗體能夠對燒傷合併葡萄球菌感染的肺損傷起到明顯的保護作用,同時金黃色葡萄球菌產生的腸毒素SEB能刺激淋巴細胞大量活化,促使炎症細胞因子產生顯著增加,致使炎症細胞浸潤,組織壞死,尤其是肺組織中的中性粒細胞聚集更加明顯,而腎臟有儲蓄和排泄腸毒素的功能,所以毒素對腎臟的損傷也較明顯,以至產生對全身其他各器官組織的損傷作用,最後發展到多個器官功能障礙,危及患者生命。
川崎病一般好發於3個月~6歲嬰幼兒,主要臨床表現為全身性多發性動脈炎,尤以冠狀動脈的損害最為常見,嚴重者危及患兒生命,該病的病因還不清楚,但是有研究認為其發病與免疫系統激活有密切關係:由於巨噬細胞、T細胞活化以及細胞因子釋放等,導致了以心血管損傷為中心多種抗原刺激后的變態反應,在這一過程中,內皮細胞的遊走與血管壁的損傷是誘發本病的最重要因素,它最終能導致冠狀動脈瘤以及內腔狹窄。
研究發現金黃色葡萄球菌腸毒素與川崎病的臨床病理密切相關,金黃色葡萄球菌廣泛存在於人體各部位,由於幼兒對其抵抗力差,作為條件致病菌合併感染在臨床上很常見,感染后金黃色葡萄球菌產生的腸毒素作為超抗原能激活大量的淋巴細胞,產生大量的細胞因子,參與β細胞多克隆活化,使免疫球蛋白合成增加,產生自身抗體,同時可誘導粘附分子在血管內皮細胞上的表達,導致內皮細胞的損傷及遊走,這些因素是導致川崎病發生的重要原因。
金黃色葡萄球菌腸毒素能夠以MHC非限制性及TCRγβ特異性的方式激活大量(為普通抗原的數千倍)T細胞並使其增殖。由此引發的應用SE作為超抗原治療癌症也在積極的研究中。這些具有生物活性的SE通過活化大量的具強大殺傷力的T淋巴細胞(CD4+和CD8+),使其增加釋放細胞因子(IL-1,IL-2,TNFα和INF-γ等),通過特異的抗原決定簇與腫瘤細胞結合併使其凋亡。
葡萄球菌腸毒素可用於生物戰劑,其氣霧劑吸入后造成多器官損傷,嚴重者可導致休克或死亡。
因有強大的激活淋巴細胞的能力,可使淋巴細胞產生強烈的細胞毒性作用和高水平的細胞因子,如腫瘤壞死因子(TNF)-α等,對腫瘤細胞具有強大的殺傷作用。有人研究SE在治療腫瘤中的作用,已有相關的臨床藥物出現。
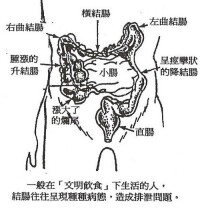
腸胃結構
腸道是人體最大的免疫器官和最重要的排泄器官;結腸是整個消化過程的最後一站,它先把經胃、腸消化后的食物中的礦物質、營養和額外水份吸收,然後把毒素和廢物排出體外。但是,結腸內有許多彎折和皺摺,甚至憩室,容易積存和殘留很多殘渣。
體內所有的組織都會受自身中毒的影響。毒素如果侵入神經系統,患者會感到煩燥和沮喪;如果侵入心臟,會感到虛弱;如果進入胃部,會感到胃部腫脹;如果進入肺部,會有口臭;如果迴流至皮膚,皮膚便會變得灰黃,而且起皺紋;如果它迴流至腺體,患者會感到疲倦、缺乏活力和性慾,未老先衰。自身中毒是導致許多嚴重疾病的一個重要因素。
營養斷食期間,喝Neera檸檬飲料幾乎沒有排泄物,由於腸道蠕動減少,容易振動摩擦腸壁,迫使摺疊處長年積累的宿便脫落,所以,晚間要服用配送的清腸茶,以促進每天有排泄;對便秘嚴重的,可能需要服用草本通便丸;有結腸憩室的,需要配合浣腸水療。
浣腸水療是用高度凈化的體溫水,以一定的壓力,緩緩送入結腸之中,用水幫結腸做運動,水流刺激大腸肌肉收縮,同時稀釋、軟化結腸內的糞便,把結腸之中的毒素、氣體和宿便大量地排出體外。洗腸過程中,治療師會輔導你深呼吸、做按摩、協助結腸運動,當糞便隨排水經過一條透明管道時,躺著的洗腸者自己看得見。
金黃色葡萄球菌
Sheahan等給恆河猴餵食含SE的溶液,觀察到類似於人的腹瀉和嘔吐等反應。利用猴進行的動物學試驗,準確性高,但靈敏度低,猴的來源困難,成本高,有時因個體差異對一份樣品的檢測需要幾隻猴試驗才能確定,故極大地限制了本方法的應用。
採用幼貓作腸毒素試驗觀察其嘔吐反應時,因葡萄球菌產生的其他非腸毒素類產物也可致幼貓嘔吐易產生假陽性,特異性不強。此外,小鼠、家兔、豬、狗等其他動物均對SE不敏感或感應性差,無特異性,實用價值低。總之,動物試驗因結果判斷直觀,準確,在某些情況下可採用,但由於實驗動物來源困難,靈敏度低,檢測結果不夠理想等使其應用受到極大的限制,常採用免疫血清學方法檢測SE。
1968年,Momrae等用RIA檢測SE獲得成功,此後,很多實驗室利用RIA檢測培養液和食品提取的腸毒素。放射免疫測定法(Radioimmunoassay, RIA)是建立在標記抗原和非標記抗原對特異性抗體的競爭性抑制反應基礎上的,可以將放射性同位素I125等標記到特異性抗體上,用於檢測未知樣品中的SE;或者將同位素標記到腸毒素抗原上,標記SE與未標記SE和特異性抗體發生競爭結合,被檢材料中未標記的SE可抑制標記SE與相應抗體的結合,抑製程度與標本中SE的濃度成正比,然後測定複合物中標記腸毒素的減少程度,可對檢樣中同型腸毒素進行定量檢測。
RIA法將同位素測定的高靈敏性和抗原抗體反應的高度特異性有效結合起來,特異性強,敏感性高,檢測樣品中各型SE可達1ng/mL。但RIA需要有放射性廢物處理系統,也需要複雜放射性計數設備,從事RIA的工作人員還必須進行專門培訓,熟悉技術,還必須有從事該項工作的許可證,這些均限制了RIA法的使用。
酶聯免疫吸附試驗(Enzyme linked immunosorbent assay,ELISA) ELISA是利用酶標記的抗原或抗體,在固相載體上進行抗原或抗體的測定。該法自1971年建立后被廣泛應用於多種疾病的免疫血清學檢測。常用雙抗體夾心法檢測SE,其靈敏度為1ng/mL,檢測速度快,4h就可出結果。一般樣品(如食品)不需要進行任何前處理,可直接用於SE的檢測,已有商品化的ELISA試劑盒,如RIDASCREEN SET(R4101)、TECRA Staph enterotoxin ID Kit等,用於檢測SE中的A、B、C、D和E等。Schotte報道一種改良的ELISA方法—快速免疫色析手工操作法(Rapid immunochromatographicbased hand-hold assay)能夠在15min之內檢測出500pg/ml的SE。
ELISA具有RIA的靈敏度和各種免疫瓊脂擴散法的普遍性與廣泛性,無需特異設備,克服了放射免疫檢測法的缺點,費用較低。由於此法敏感、簡便、快速、技術人員不需進行特別訓練,並能分型,是目前較為適用於檢測SE的方法。
聚合酶鏈反應技術(Polymerase Chain Reaction,PCR)PCR是一種在體內模擬自然DNA複製過程,對特定的DNA或DNA片段進行快速擴增的方法。1991年,Johnson等最先設計八對寡核苷酸引物,分別用於檢測從臨床標本和食品中分離到的產A-E型葡萄球菌腸毒素、TSSTL和表皮剝脫毒素A和B的88株葡萄球菌。隨後,Wilson等用PCR方法檢測了乾燥脫脂奶粉中的葡萄球菌腸毒素的基因entB,entCI和耐熱核酸酶基因。1998年,Becker等設計一種多重PCR-EIA法,一套用於檢測腸毒素A~E(entA、entB、entC、entE)基因,另一套用於檢測表皮剝脫毒素(eta、etb)基因和中毒性休克綜合症毒素(tst)基因。PCR技術除了具有核酸分子雜交的優點如特異性強,可從基因水平進行診斷和同時檢測大量樣品等外,比核酸分子雜交更加敏感,更加快速和更加簡便,且易自動化操作。
