甲基丙二酸尿症
多種原因所致體內甲基丙二酸蓄積的總稱
甲基丙二酸尿症(methylmalonicaciduria)或甲基丙二酸血症(methylmalonicacidemia)是先天有機酸代謝異常中最常見的病種,是多種原因所致體內甲基丙二酸蓄積的總稱,於1967年首次被報道。近年來,其病因、診斷、治療與遺傳學機制逐步明確,隨著質譜分析技術的普及,本症的流行病學資料亦不斷更新。據報道日本發病率為2/9780,2/102200至2/16246,義大利1/61775,中國發病情況不詳。
甲基丙二酸尿症,又稱甲基丙二酸血症,英文名字:methylmalonic academia,MMA屬常染色體隱性遺傳。臨床主要表現為早嬰期起病,嚴重的間歇性酮酸中毒,血和尿中甲基丙二酸增多。根據甲基丙二酸輔酶A變位酶缺陷分為完全缺失Mut0和部分卻失Mut1型,其中最嚴重的是Mut0型。
1、甲基丙二酸尿症是遺傳性有機酸代謝異常中最常見的疾病,為常染色體隱性遺傳病;
4、目前已發現7種不同的酶缺陷類型,根據VB12試驗治療是否有效,臨床分類為VB12有效型與無效型;
7、對VB12有效型患兒採用VB12長期維持劑量,每周肌注1次 1 mg 或每天口服10~20 mg;
8、對重症患兒尚應給予低蛋白、高熱量飲食控制,使血、尿甲基丙二酸濃度維持在理想範圍;
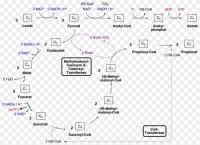
甲基丙二醯CoA變位酶的輔酶
除上述遺傳缺陷外,轉鈷胺素Ⅱ缺陷、慢性胃腸與肝膽疾病、長期素食、特殊藥物治療可導致維生素B12缺乏,引起甲基丙二酸尿症。母親長期維生素B12攝入不足造成胎兒維生素B12缺乏,不僅引起母親惡性貧血,亦將導致嬰兒繼發性甲基丙二酸尿症,造血功能障礙,神經系統發育異常。
甲基丙二酸是甲基丙二醯輔酶A的代謝產物,正常情況下在甲基丙二醯輔酶A變位酶及維生素B12的作用下轉化生成琥珀酸,參與三羧酸循環。甲基丙二醯輔酶A變位酶缺陷或維生素B12代謝障礙導致甲基丙二酸、丙酸、甲基枸櫞酸等代謝物異常蓄積,琥珀酸脫氫酶活性下降,線粒體能量合成障礙,引起神經、肝臟、腎臟、骨髓等多臟器損傷。患者腦組織病理分析可見腦萎縮、瀰漫性神經膠質細胞增生、星形細胞變性、腦出血、蒼白球壞死、丘腦及內囊細胞水腫,均與線粒體功能不良有關。
曾有病理解剖發現患兒神經膠質細胞反應性增生,深部皮質、小腦顆粒層和膠質細胞發育不良,小腦、腦幹、頸髓髓鞘化延遲。另有屍檢發現腎臟、肺部血栓性毛細血管病、肝臟瀰漫性脂肪變性、骨髓巨幼紅細胞增生、嚴重胃黏膜發育不良伴胃炎。這些表現部分為胎兒時期代謝異常所致損害,部分為出生後有機酸毒性損害所致。
mut0型患者起病最早,80%在生后數小時至1周內發病,類似急性腦病樣癥狀,如:拒乳、嘔吐、脫水、昏迷、驚厥、酸中毒、酮尿、低血糖,早期死亡率極高,預后不良。mut-及Cb1A和Cb1B型患者多在生后1月後發病,Cb1C和Cb1D在新生兒期至成年發病者均有報道,Cb1F報道很少。
部分患者呈急性發病或間歇性發病,發熱、感染、飢餓、疲勞、外傷等應激狀態下機體能量需求增加,高蛋白飲食、輸血等因素引起甲基丙二酸前身物質蛋氨酸、蘇氨酸、異亮氨酸、纈氨酸蓄積,丙戊酸、大環內酯類藥物導致左旋肉鹼消耗,甲基丙二酸排泄障礙,引起急性代謝紊亂。
患者臨床表現常無特異性,常常被誤診為一般圍產期腦損害、敗血症、急慢性腦病或腦變性病,常見餵養困難、嘔吐、呼吸急促、驚厥、肌張力異常、嗜睡、智力、運動落後或倒退,急性期可見昏迷、呼吸暫停、代謝性酸中毒、酮症、低血糖、高乳酸血症、高氨血症、高甘氨酸血症、肝損害、腎損害,嚴重時腦水腫、腦出血。患者神經系統異常各不相同,多於嬰兒期出現智力、運動落後,肌張力低下,變位酶缺陷患者常較鈷胺素代謝異常患者神經系統損害出現早,並且嚴重。少數鈷胺素代謝異常所致良性甲基丙二酸尿症患者可於成年後發病,甚至終身不發病。嚴重患者由於免疫功能低下,易合併皮膚念珠菌感染,常見口角、眼角、會陰部皸裂和紅斑。隨著代謝紊亂的控制,患者皮膚損害逐漸恢復。
甲基丙二酸尿症常導致多臟器損害。患者肝臟常明顯腫大,肝功能異常。骨質疏鬆較為常見,嚴重時可導致骨折。腎小管酸中毒、間質性腎炎、高尿酸血症、尿酸鹽腎病、遺尿症等慢性腎損害也屢見報道。嚴重患者合併溶血尿毒綜合征,表現為微血管性溶血性貧血、血小板減少、腎功能衰竭、高血壓。患者血液系統異常多見巨幼細胞性貧血、粒細胞減少,血小板減少,嚴重時甚至出現骨髓抑制。少數患者合併口炎、舌炎、角膜潰瘍、一過性糖尿病等異常。甲基丙二酸尿症嬰兒常表現為相似面容,如:高前額、寬鼻樑、內眥贅皮、三角形嘴。患者個體差異很大,即使相同缺陷的同胞亦輕重不同。
甲基丙二酸尿症患者腦CT、MRI掃描常見對稱性基底節損害,以蒼白球損害為主。嬰幼兒患者白質發育落後、年長兒腦白質變性出現較早,隨病情進展出現瀰漫性腦萎縮。患者生后第1個月腦影像學可正常或白質變薄,1歲左右可發展為中到重度腦萎縮及白質發育落後。典型患者可見瀰漫性幕上白質水腫和髓鞘化不良,亦可因瀰漫性的顱內血管硬化導致腦積水。白質損傷可能與甲基化功能不良、非生理性的脂肪酸毒性有關。神經膠質細胞的增生與高半胱氨酸對內皮的毒性有關。
(1)甲基丙二醯輔酶A變位酶缺乏已報道100餘例。
臨床治療
(2)甲基丙二醯輔酶A變位酶和甲基四氫葉酸
同型半胱氨酸甲基轉移酶聯合缺乏已報道數十例遺傳性聯合性甲基丙二酸血症和同型胱氨酸尿症,缺陷為ch1C,cblD, cblF。cblC缺陷者臨床表現變異較大,但均以神經系統癥狀為主。早發病例在生后兩月出現癥狀,表現為生長發育不良、餵養困難或嗜睡。遲發病例可在4~14歲出現癥狀,可有倦怠、譫妄和強直痙攣,或痴獃、脊髓病等。大多數病例均有血液系統異常,如巨幼紅細胞和巨紅細胞貧血、多形核白細胞核分葉過多和血小板減少等。患者血清鈷胺素和葉酸濃度均正常。cblD缺陷者發病較晚,表現為行為異常、智能落後和神經肌肉病變,無血液系統異常。數例cblF缺陷者均在生后兩周出現口腔炎、肌張力低下和面部畸形,部分有血細胞形態異常。本症患者除有特徵性甲基丙二酸血症和同型胱氨酸尿症外,部分病例有低甲硫氨酸血症和胱硫醚尿症。
由於個體差異較大,臨床誤診率較高,對於原因不明的嘔吐、驚厥、酸中毒、肌張力異常、發育落後、呼吸困難等患兒應及早進行有關檢查,尿酮體測定、血氣分析、血氨、血糖、心肌酶譜等一般生化檢查均有助於診斷。氣相色譜2質譜聯用分析尿、血、腦脊液有機酸定量檢測是確診本症的關鍵方法。正常人尿甲基丙二酸濃度<2mmol/mol·肌酐,24h的排出量<5mg,在甲基丙二醯輔酶A變位酶缺陷的患者尿甲基丙二酸濃度為270~13000mmol/mol·肌酐,24h總量可達240~5700mg。由於丙酸蓄積,患者尿32羥基丙酸和甲基枸櫞酸濃度亦明顯增高。經治療後患者尿甲基丙二酸排出可明顯減少。正常人血漿難以檢出甲基丙二酸,患者可達200~2500mmol/L。腦脊液甲基丙二酸濃度與血漿濃度接近。應注意排除新生兒期其它原因引起的酮症酸中毒、鈷胺素缺乏和其他原因所致同型半胱氨酸血症。
本症的病型分析需依賴皮膚成纖維細胞、淋巴細胞、肝組織纖維母細胞酶學分析或基因診斷。通過胎盤絨毛細胞、羊水細胞酶學檢查、母親尿液及羊水甲基丙二酸測定,可進行本症的產前診斷,國內外取得了成功的經驗。曾有患兒經產前檢查證實為脫氧腺苷鈷胺素合成酶缺陷,在出生前接受鈷胺素治療,得到了有效的控制。
本症急性期的治療應以補液、糾正酸中毒為主,必要時進行腹腔透析或血液透析,同時,應保證熱量及液體供給以減少機體蛋白分解,必要時給予小量胰島素,限制天然蛋白質的攝入。鑒於重症患兒或代謝性酸中毒急性發作期死亡率極高,臨床高度懷疑時,可在確診前進行治療,如中止蛋白質攝入、靜脈補液、肌注大劑量維生素B12。
對所有甲基丙二酸尿症患者應首先進行大劑量維生素B12試驗治療,1mg/d肌肉注射,3~5d,對照治療前後尿甲基丙二酸濃度,判斷對維生素B12的反應性。通過大劑量維生素B12試驗治療不僅可以爭取治療時機,挽救維生素B12反應型患者,亦有助於病型診斷,指導長期治療。
維生素B12無效型以飲食治療為主,理想方式為限制天然蛋白質,補充去除異亮氨酸、纈氨酸、蛋氨酸、蘇氨酸的特殊治療奶粉,嬰幼兒期天然蛋白質每日攝入量應控制在1.0~1.2g/kg。維生素B12有效型其維生素B12長期維持劑量為1mg每周至每月肌肉注射1次或每日口服甲基鈷胺素500~1000μg,中等量蛋白質攝入,使血、尿甲基丙二酸濃度維持在理想範圍。
由於甲基丙二酸、丙酸等有機酸蓄積,生成相應酯醯化肉鹼,導致肉鹼消耗增加,補充肉鹼可促進酯醯肉鹼排泄,增加機體對自然蛋白的耐受性,不僅有助於急性期病情控制,亦可有效地改善預后。急性期可採用靜脈或肌內注射肉鹼每日100~200mg/kg,緩解期每日30~60mg/kg,長期維持。對於合併同型半胱氨酸血症的患者,應給予甜菜鹼(betaine)補充治療(1000~3000mg/d),降低血液同型半胱氨酸濃度,改善患兒神經系統情況。
該病的預后取決於病型、發現早晚及長期治療的合理性。但有人認為發病的早晚與中樞神經系統的預后及生命的長短無關。鈷胺素合成缺陷者發病較變位酶缺陷者晚,經過治療后大多能存活。mut0型預后最差,維生素B12不反應型預后不佳,Cb1A型預后最好。神經功能損害的輕重與高氨血症、代謝性酸中毒等持續時間的長短有關,通過早期診斷和治療可降低死亡率,減少神經系統後遺症。