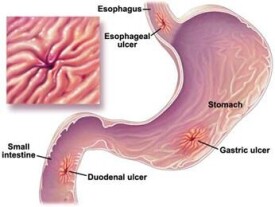
兒童消化性潰瘍
兒童消化性潰瘍
兒童消化潰瘍分為原發性和繼發性兩類,6歲以下患兒的原發性潰瘍主要是胃潰瘍,以後十二指腸球部潰瘍佔優勢,小兒胃潰瘍年齡偏小(新生兒也不能倖免),十二指腸球部潰瘍年齡偏大。男性兒童的發生率高於女性兒童,為3∶1~6∶1。10歲以下的兒童潰瘍病為繼發性潰瘍。消化性潰瘍在兒童中發生情況相對較少,兒童住院病人2500人中有1人因消化性潰瘍而住院。因兒童消化性潰瘍缺乏典型癥狀,各年齡階段的臨床表現差並較大,易發生誤診和漏診。
2.臨床分型Tudor在分析了378名病例,將兒童消化性潰瘍分為4種類型。
(1)原發性急性潰瘍:潰瘍病以出血或穿孔的形成為主要或惟一臨床表現。多見於2歲以下的嬰兒。
(3)慢性潰瘍:癥狀接近成人,可以發生出血或幽門梗阻併發症。
(4)應激性潰瘍。
1.食物與不良生活習慣飲食與潰瘍病的流行和發病規律的關係。但認為飲食不當、缺乏規律或進食時不經細嚼可增加潰瘍病的危險性。在遺傳、精神等其他因素的作用下,又進食大量辛辣等刺激性食物,均可誘發胃炎,進而形成潰瘍。因此,從兒童期養成規律進食的良好生活習慣,是預防該病的一個重要方面。抽煙可導致幽門括約肌鬆弛,引起膽汁反流,飲酒可使胃黏膜抗力降低而誘發潰瘍。小兒抽煙、飲酒習慣極少,但被動吸煙是否也能起到同樣作用而誘發潰瘍,應引起足夠重視。
2.胃酸-胃蛋白酶胃酸-胃蛋白酶對胃的自身消化作用導致消化性潰瘍的形成。胃酸是由壁細胞分泌的。壁細胞表面至少有3種興奮性受體,即胃泌素、乙醯膽鹼和組織胺受體。3種受體任何一種受到刺激均可導致胃酸的分泌。其泌酸機理是通過“H+、K+-ATP酶”即“酸泵”來實現的。鹽酸的分泌機制:HCI中的H+來源於壁細胞內物質氧化代謝所產生的水。水解離成H+和OH-,H+通過存在於細胞內小管膜上的H+泵,主動轉運入小管內。Cl-來自血漿,血漿中的Cl-通過擴散和易化擴散的方式進入壁細胞后,再經細胞內小管膜上的氯泵被泵入小管內,H+和Cl-的分泌一般是耦聯的,H+和Cl-在細胞內小管中形成HCl,隨後進入腹腔。
迷走神經興奮胃酸分泌增加,部分消化的蛋白質可刺激腸黏膜分泌某種物質直接或通過胃泌素促進胃酸分泌,即為胃酸分泌的腸相。有人認為還有其他未知的物質(非胃泌素物質)也能促進胃酸的分泌。各種內外因素能啟動胃泌酸機制者,均可使胃酸增多,進而導致潰瘍的發生。潰瘍病人的泌酸能力亢進,尤其是十二指腸潰瘍患兒。
新生兒胃、十二指腸潰瘍與胃分泌物的酸度較高有關。新生兒在初生10天里胃遊離鹽酸甚高,第4天達高峰。嬰兒在第1年內胃酸保持較高水平,至4歲時下降,4歲后又逐漸回升至成人水平。但與成人不同的是總酸量(2%~5%)與遊離鹽酸量(0.5%)差距較大。胃酸過多和胃運動過度對兒童消化性潰瘍的發生可能較成人更為重要。在高胃酸的條件下,胃蛋白酶對胃、十二指腸黏膜的蛋白產生水解消化作用,導致潰瘍的形成。但胃蛋白酶在10歲以下兒童並不重要,因其10歲以後方接近成人。總之,由於胃酸、胃蛋白酶侵入黏膜的力量與胃、十二指腸黏膜本身的抵抗力之間失去平衡而致消化性潰瘍的發生。
3.精神因素在150年前Beaumont即精確地描述了1例胃瘺病人情緒變化對胃黏膜及其分泌的影響:興奮時黏膜充血,分泌增加,胃運動加強;精神抑鬱時黏膜蒼白,分泌減少,胃運動減弱。研究也證實胃液的分泌會受情緒和生物反饋控制的影響。消化性潰瘍的精神因素學說認為,長期受到心理應激如精神創傷時,胃黏膜抵抗力下降可誘發潰瘍的形成。隨著醫學模式的轉變,人們越來越認識到精神因素在潰瘍病中的致病作用。兒童潰瘍病與精神因素也有顯著關係。在成人病例中,不少是開始於幼年時期的某種劣性環境和精神創傷誘發的。
4.遺傳因素消化性潰瘍的發病與遺傳因素密切相關。肯定與遺傳有關的消化性潰瘍是Ⅰ型多發性內分泌腺瘤症(MEAⅠ型或稱Wermer綜合征)和Neuhauser綜合征(十二指腸潰瘍、眼球震顫和肌震顫)。多數潰瘍病可能為多基因遺傳。下列事實提示其與遺傳密切相關。
(l)家族發病傾向:慢性消化性潰瘍者親屬患潰瘍病的機會要比一般人群大2.5~3倍,而且胃潰瘍患者的子女易患胃潰瘍,十二指腸潰瘍患者的子女易患十二指腸潰瘍。有人統計62例小兒病例中,約1/3潰瘍病患者有明顯的家族史,同卵雙生子之一患消化性潰瘍,另一個易患同種潰瘍;而非同卵雙生子則非如此。此點說明遺傳因素對消化性潰瘍發病中的作用。
(2)血型傾向:研究發現十二指腸潰瘍病與2種血型基因特性有關:ABO血型和血型物質ABH分泌狀態。血型O的人潰瘍病的發生較血型A、B或AB者高1.4倍。根據血型物質分泌入唾液及其他體液與否,把人群分為分泌者(占正常人80%)和非分泌者兩大類。非分泌者較分泌者患十二指腸潰瘍可能高1.5倍。
(3)HLA抗原與消化性潰瘍:國內外學者從組織相關抗原的角度來分析十二指腸潰瘍,發現屬HLA-B的頻率較高,如北京地區漢族人中十二指腸潰瘍患者HLA-B5頻率為36.07%(對照組12.5%)。另外,HLA-A24,HLA-B35也與潰瘍的發生有關。
(4)高胃蛋白酶原血症傾向:通過血中和尿中胃蛋白酶元的研究發現,潰瘍病患者致潰瘍的泌酸腺量及其分泌胃酸、胃蛋白酶的能力存在遺傳學上的異常。血清中胃蛋白酶無濃度增高者容易發生十二指腸潰瘍。高胃蛋白酶原屬常染色體顯性遺傳。其子女中發生高組Ⅰ胃蛋白酶原血症的機會為50%,同樣伴有十二指腸潰瘍者約為25%。可見壁細胞群及其泌酸能力受遺傳因素控制,在後天環境因素的影響下導致高胃酸分泌和十二指腸潰瘍的形成。總之,消化性潰瘍的發生與遺傳有一定關係,但尚不能完全用遺傳來解釋所有的潰瘍病。
5.藥物腎上腺皮質激素和非甾體類藥物(NSAID)可引起急、慢性胃及十二指腸炎和潰瘍。激素和非甾體類藥物引起潰瘍的相對危險性各學者報道不一,一般為正常人群的2~7倍。原有某種胃部疾病和消化功能紊亂者更宜罹患。非甾體類藥物抑制環氧化酶活性從而降低局部前列腺素的產生,使胃黏液分泌減少,黏液層厚度減少;抑制十二指腸分泌重碳酸鹽,血管收縮,膽鹽損傷增加,從而削弱了胃、十二指腸的黏膜屏障作用。同時自由基的形成增加,白細胞三稀的產生以及其他有害刺激作用,導致潰瘍形成。如同時吸煙或飲酒,可使非甾體類藥物的致潰瘍作用明顯加強。
(2)繼發性高胃泌素血症:由於慢性萎縮性胃炎使壁細胞數量減少,泌酸能力減弱,胃液胃酸含量降低(pH>4),通過反饋機制,胃G細胞分泌大量胃泌素,而產生高胃泌素血症。
(3)胃泌素瘤:又稱Zollinger-Ellison綜合征。發生於胃的G細胞的腫瘤為Ⅰ型,發生於胰島非β細胞瘤或其他異位腫瘤為Ⅱ型。其表現為:①胃酸分泌及胃液極度增加;②上消化道反覆出現多發難治的潰瘍,易穿孔;③高胃泌素血症占潰瘍病的0.1%~0.15%,是消化性潰瘍的重要致病因素。隨著血胃泌素監製技術的不斷提高,將有更多的隱匿型病例被發現。多在兒童期發病,故兒童十二指腸潰瘍患者應想到這一可能性。
7.感染因素
(1)幽門螺桿菌(Hp)感染:1983年Warren和Marshall從慢性胃炎病人胃黏膜中分離到幽門螺桿菌(Helcobacterpylori,Hp)以來,國內外做了大量研究工作。張振華等(1985)首先報道分離培養成功。幽門螺桿菌是一種呈“S’形或“U”形彎曲的革蘭陰性桿菌,特異性的寄居於胃黏膜的黏液層下面、上皮細胞表面和十二指腸、食管的胃上皮化生區。大量的資料表明,幽門螺桿菌與慢性胃炎、消化性潰瘍有高度的相關性。幽門螺桿菌感染遍布世界各地,屬於感染率較高的國家。小兒檢出率報道不一,國外報道占胃鏡檢查兒童的10%~20%。感染多發生於年長兒,一般在6歲以上,無性別差異。河南醫學科學研究所在河南輝縣一個鄉571例自然人群胃鏡普查中發現,幽門螺桿菌感染率男性為72%,女性為63%;15~20歲組為53.6%,成年組為76%。幽門螺桿菌檢出陽性者中,6.4%胃黏膜正常,其餘9.36%呈慢性胃炎改變。北京醫科大學在山東牟平縣胃癌高發區347例無癥狀者胃鏡活檢中幽門螺桿菌檢出率73.7%,10~30歲者為50%。30~50歲者75%,50歲后降至42%~44%;值得注意的是胃黏膜正常者中未檢出幽門螺桿菌。北京醫科大學第三附屬醫院對47名無癥狀的11~14歲兒童進行檢查,幽門螺桿菌檢出率為52.5%;有慢性胃炎者為40%~80%,活動性胃炎者為90%,胃潰瘍者為60%~80%;十二指腸潰瘍70~90%。上海潘志君等用檢測幽門螺桿菌抗體IgGEMLIA(間接酶聯免疫吸附實驗)法檢測168例經胃鏡確診的血清幽門螺桿菌抗體,在A型胃炎、B型胃炎、胃與十二指腸潰瘍患者中的檢出率分別為11%、84%、86%和90%。說明幽門螺桿菌與B型胃炎與消化性潰瘍有密切關係。另對180例體檢者和38例新生兒進行抗體檢查,發現10歲以下兒童檢出率為25%,10歲后隨年齡增長,達70%,70歲后檢出率又降為39%。新生兒幽門螺桿菌抗體與成人相近,為53%。而10歲后幽門螺桿菌抗體降為25%,說明此種抗體可通過胎盤進入胎兒體內,10歲以後幽門螺桿菌抗體檢出率又上升,與西方國家報道在20歲后幽門螺桿菌抗體才增加的結論不同,這可能與胃炎發病率高、發病年齡小有關。胃與十二指腸潰瘍胃竇黏膜幽門螺桿菌檢出率為60%~100%。說明幽門螺桿菌是成人和兒童消化性潰瘍的重要致病因素,而且幽門螺桿菌的持續存在與潰瘍的頑固不愈和複發有關。幽門螺桿菌引起潰瘍的機理大致與以下幾點有關:①幽門螺桿菌在胃、十二指腸胃上皮化生區生長,破壞黏膜的正常結構和防禦機制。②幽門螺桿菌可能含大量尿素酶,使尿素水解產生氨,影響上皮細胞周圍環境,阻斷H+從胃底腺正常進入胃腔,從而使H+發生逆擴散,使潰瘍形成。③細胞代謝使細胞通透增加,蛋白滲出,導致胃、十二指腸黏膜損傷。④幽門螺桿菌寄生或其產生的代謝產物使胃泌素、組織胺釋放增加而致酸分泌增加。國外對志願者口服幽門螺桿菌,已獲人類實驗感染幽門螺桿菌2例成功,說明幽門螺桿菌可以感染正常的胃黏膜引起胃的炎症,進而形成潰瘍。
8.胃腸激素與消化性潰瘍消化道被認為是身體內最大的、最複雜的內分泌器官,分泌多種激素。有些不僅作用於消化道,也作用於其他組織器官。這些激素在胃功能調節中發揮重要作用,與潰瘍病發生密切相關。在實驗性潰瘍中發現,神經降壓素(NT)、β-內啡肽、鈴蟾肽(蛙皮素)(Bombisine,Bon)、降鈣素(GRP)對實驗性潰瘍有保護作用;促甲狀腺激素釋放激素、血管活性腸肽具有致潰瘍作用;而生長抑素(SS)、緩激肽、P物質、胃泌素、膽氨酸腦啡肽、亮氨酸腦啡肽、促性腺激素釋放激素、生長激素釋放激素和黑色素細胞釋放抑制因子與潰瘍發生無關;還有一些激素也促進胃酸分泌,而有一些則抑制胃酸分泌。
9.多巴胺(DA)與消化性潰瘍在1965年Strang即注意到帕金森病外周多巴胺(DA)含量少,同時合併潰瘍者較對照組多;相反,精神分裂症病人中樞多巴胺含量高,潰瘍病發病率則較低。多巴胺與潰瘍病的關係已被動物實驗所證實。半胱胺可致成十二指腸潰瘍模型,若在腦室注射多巴胺,則可使潰瘍減輕,且中樞多巴胺含量減少的程度與潰瘍的嚴重程度成正比。使用多巴胺受體激動劑對實驗性潰瘍有保護作用,而使用多巴胺阻滯劑則可促進潰瘍形成。臨床應用多巴胺受體激動劑溴隱亭治療十二指腸潰瘍獲得了成功。亦有應用L-多巴治療潰瘍獲較好效果的報道,均證明了多巴胺與潰瘍病的關係。
10.自由基與消化性潰瘍近年來許多學者在潰瘍病變周圍黏膜中發現自由基含量明顯升高,並認為其與炎症的發生、發展和潰瘍的形成有關。
11.其他易併發潰瘍的疾病當患有某些疾病時,患消化性潰瘍病的幾率可明顯高於正常人群。如慢性肝炎、肝硬化、膽道疾病、胰腺疾病、慢性腎功能衰竭、甲狀旁腺功能亢進症等。以上疾病均可致消化道功能紊亂,而易患潰瘍。肝硬化時,由於門脈系統淤血,故胃腸消化功能降低。甲狀旁腺功能亢進時,持續大量的甲狀旁腺素可直接刺激胃泌素釋放增多;而尿毒症患者除了存在繼發性甲狀旁腺功能亢進,大量的甲狀旁腺素致的胃泌素增多外,由於腎實質破壞又使胃泌素降解減少,故血中胃泌素含量增多,從而可刺激胃酸分泌,促進潰瘍的形成。
2.病理改變胃潰瘍多發於胃小彎,尤以胃竇小彎側胃角附近多見,胃底或胃大彎側較少見;潰瘍常為單個,約5%的病倒為多發。潰瘍呈圓形或橢圓形,直徑大多在2cm以內。十二指腸潰瘍則以十二指腸球部前壁或後壁多見,形態與胃潰瘍相似,較胃潰瘍小而淺,直徑多在1cm以內。潰瘍一般深至黏膜肌層,邊緣光整,周圍黏膜常有炎性水腫,活檢切片用HE染色,常可找到幽門螺桿菌。潰瘍基底可分為4層:表面第1層為含白細胞、紅細胞的纖維素滲出物,第2層為纖維素樣的壞死組織,第3層為含血管的炎性肉芽組織,第4層為緻密的纖維組織瘢痕(只見於慢性潰瘍)。潰瘍深者可累及胃壁肌層,潰破血管時引起出血,穿破漿膜時則引起潰瘍穿孔。
1.癥狀與體征凡有下列之一或更多項者應想到潰瘍病的可能性。
(2)複發性上腹或臍周不適或疼痛、壓痛,除外腸寄生蟲感染及其他疾患。
(3)有潰瘍病家族史,並有上消化道癥狀者。
3.HP感染診斷標準
(1)細菌培養陽性。
(2)組織切片染色見到大量典型螺桿菌者。
(4)2周內服用抗生素者,上述檢查可呈假陰性。
2.幽門螺桿菌及抗螺旋桿菌抗體IgG的檢測由於大量的資料證明幽門螺桿菌與消化性潰瘍的發病和複發有著密切的關係,因此有作者主張檢測血清抗幽門螺桿菌抗體,或取潰瘍旁及胃竇黏膜直接檢菌,以輔助診斷。並將幽門螺桿菌或幽門螺桿菌抗體陽性的潰瘍命名為幽門螺桿菌相關潰瘍。
(1)組織細菌學檢查:胃鏡取活組織胃、十二指腸黏膜、經特殊銀染色,電鏡直接檢菌。
(3)胃液尿素酶:由於幽門螺桿菌侵入體后存在於胃黏膜上皮細胞表面、黏膜隱窩內或聚集在細胞連接處附近。在其生長繁殖中產生大量尿素酶,故胃液尿素酶的含量升高。用特殊藥盒測定胃液尿素酶的含量,間接診斷幽門螺桿菌感染。
2.內鏡檢查是確診潰瘍病、評定潰瘍活動程度、確定有無Hp感染及評價療效的最佳方法。
(1)根據部位分型:①胃潰瘍;②十二指腸潰瘍;③複合性潰瘍:胃和十二指腸潰瘍並存。
(2)根據內鏡所見分期:①活動期:潰瘍基底部有白色或灰白色厚苔,邊緣整齊,周圍黏膜充血、水腫,有時易出血;水腫消退,呈黏膜向潰瘍集中。十二指腸潰瘍有時表現為一片充血黏膜上散在小白苔形如霜斑,稱“霜斑樣潰瘍”。②癒合期:潰瘍變淺,周圍黏膜充血水腫消退,基底出現薄苔,薄苔是癒合期的標誌。③瘢痕期:潰瘍基底部白苔消失,遺下紅色瘢痕。以後紅色瘢痕轉為白色瘢痕,其四周黏膜輻射狀,表示潰瘍完全癒合,可遺留輕微凹陷。
3.胃電圖(EGG)根據現代電生理知識,人的每個臟器乃至體表都有電活動存在。現研究透徹並已得到廣泛應用的如心電、腦電等。潰瘍、瘢痕伴隨胃平滑肌運動而產生的生物電活動稱為胃電;用皮膚表面電極把這種胃電活動從胃區體表(膠壁)引出,並用胃電圖儀記錄下來,即為胃電圖。10年來,胃電圖臨床應用研究發展很快,認為該檢查無創傷,適應於任何年齡和胃及十二指腸各種疾病。用於病員的初選和不適應或拒絕接受胃鏡、X線檢查者有較大臨床意義。特別對兒童消化潰瘍判斷有一定價值。表現如下:
(1)胃炎:餐前或餐后升高的幅值在100uv左右,頻率3次/min以下,波形以低幅波為主。
(2)十二指腸潰瘍:餐前或餐后也升高、降低的幅值約在160uv以下,或餐后幅值在250μr左右。頻率往往在3次/min以上。波形以低幅波或低間高波和高幅不規則波為主。
(3)胃潰瘍:胃電圖振幅餐前、餐后均在250uv以上,或餐后升高、降低的幅值在200μr左右。頻率3次/min以上。波形以低幅或低高幅兼存和高而不規則為主。
(4)胃癌:振幅高於潰瘍病幅值或低於胃炎的幅值,頻率在3次/min以下,波形高而紊亂或低平波。胃電圖與胃鏡檢查進行對照總符合率73%;其中胃炎、胃癌的符合率為80%;潰瘍病的符合率在53%~69%,個別資料中認為可達90%,但其確切的臨床價值仍有待進一步觀察研究。
4.胃癌小兒少見,可通過X線及內鏡檢查確診。
1.一般治療
(1)適當休息:在急性發作時給予體力和精神兩方面的休息,可促進癥狀緩解。嚴重者可卧床3~7天,可減少膽汁反流,緩解癥狀。
(2)飲食:少食多餐。少食可使食物刺激胃酸分泌的時間短,減輕胃竇擴張,減少胃泌素的分泌。多餐,白天可進餐4~5次。食物盡量適應病兒習慣,低脂、適量蛋白質和碳水化合物。油炸、辛辣食物應禁忌。
(3)繼發性潰瘍應積極治療原發病。
2.藥物治療消化性潰瘍藥物治療通過以下3條途徑:
(1)抑制胃酸:是消除侵襲因素的主要途徑,常用藥物有:
①H2受體拮抗劑(H2RA):有很好的抑制胃酸和抗潰瘍作用。常用的H2受體拮抗劑為雷尼替丁(ranitidine),3~5mg/(kg?d),1次/12h或睡前1次服用,療程4~8周;西咪替丁(cimitidine),10~15mg/(kg/d),1次/12h或睡前1次服用,療程4~8周;法莫替丁(famotidine),0.9mg/(kg/d),睡前1次服用,療程2~4周。上述3種葯中以雷尼替丁較好。新型的H2受體拮抗劑尼扎替丁(nizatidine)、羅沙替丁(roxatidine),兒科尚無臨床用藥經驗。
②質子泵抑製劑(PPI):質子泵抑製劑對壁細胞分泌膜內質子泵(H+-K+ATP酶)活性具有抑制作用,可明顯減少任何刺激激發的胃酸分泌,並對Hp有一定的抑制作用。奧美拉唑(omeperazole,洛賽克)0.6~0.8mg/kg,每天清晨頓服,療程2~4周,潰瘍大多數能癒合。
③前列腺素擬似品:前列腺素具有細胞保護作用,可強化胃腸黏膜防衛能力,但其抗潰瘍作用主要在於對胃酸分泌的抑制,米索前列醇(misoprostol,喜克潰)是應用於臨床的前列腺素擬似品,治療效果大致相當於H2受體拮抗劑,副作用較多,不作為常規治療藥物,主要用於NSAID服用者,預防和減少胃潰瘍的發生。
⑤胃酸中和劑:比較常用的是氫氧化鋁凝膠、復方氫氧化鋁片(胃舒平)、鋁碳酸鎂(胃達喜),復方碳酸鈣等,飯後1h服用。起緩解癥狀和促進潰瘍癒合的作用。片劑宜嚼(或研)碎后服用。
(2)強化黏膜防禦能力:
①硫糖鋁:該葯作用有3個:在潰瘍表面形成保護膜,防止胃酸侵入;降低胃蛋白酶結合酶的活性,抑制其對蛋白質分解;刺激局部前列腺素E2分泌和聚集釋放的表皮生長因子,促進潰瘍的癒合。療效相當於H2受體拮抗劑,常用劑量10~25mg/(kg?d),分4次口服,療程4~8周。
②枸櫞酸鉍鉀(膠體次枸櫞酸鉍,CBS):作用機製為:隔離潰瘍作用,保護黏膜;促進胃上皮細胞分泌黏液,抑制人體胃蛋白酶對黏液層的降解,促進前列腺素分泌,與表皮生長因子形成複合物,使生長因子聚集於潰瘍部位,從而促進再上皮化和潰瘍癒合,且具抗Hp作用。劑量為6~8mg/(kg?d),分3次口服,療程4~6周。CBS治療消化性潰瘍療效與H2受體拮抗劑相似,主要優點在於能減少潰瘍的複發率,此可能與其對Hp有殺滅作用有關。
③呋喃唑酮:作用機制是抑制機體內單胺氧化酶活性,提高體內多巴胺活性。多巴胺抑制胃酸分泌、胃運動和擴張血管,從而維持胃黏膜完整性,對胃黏膜起保護作用。劑量為3~5mg/(kg?d),分2~3次,療程2周。
④柱狀細胞穩定劑:復方谷氨醯胺(麥滋林-S)、替普瑞酮(tepredone)、吉法酯(gefarnate)等。主要用於潰瘍病的輔助用藥,尤其與抗胃酸分泌類藥物聯合應用,有促進潰瘍癒合的作用,也用於潰瘍病恢復期維持治療,防止複發。
(3)抗Hp感染:臨床常用藥物有阿莫西林(羥氨苄青霉素)30~50mg/(kg/d),甲硝唑15~20mg/(kg?d),替硝唑10mg/(kg/d),克拉黴素15~20mg/(kg/d),此外枸櫞酸鉍鉀(CBS)、呋喃唑酮等亦有抗螺桿菌的作用。
(4)治療實施:
①初期治療:H2受體拮抗劑或奧美拉唑作為首選藥物;硫糖鋁也可作為第一線治療藥物,Hp陽性患兒應同時進行抗Hp治療。
②維持治療:抗酸藥物停用后可用柱狀細胞穩定劑丙谷胺維持治療。對多次複發、癥狀持續不緩解,或伴有併發症和合併危險因素者,持續服NSAID。Hp感染未能根治者,可給予H2受體拮抗劑,或奧美拉唑維持治療。
(2)手術的選擇:
薛紅仙(1991)報道81例行纖維胃鏡檢查的小兒,檢出病例32例,浙江醫科大學(1992)對222例腹痛患兒行胃鏡檢查,發現消化性潰瘍29例,佔13.1%;吳青英報道572例行胃鏡檢查的小兒,檢出131例,佔22.8%。胃潰瘍遠較十二指腸球部潰瘍少見,二者約1∶4。10歲以下的兒童潰瘍病多為繼發性潰瘍。