共找到2條詞條名為西樂葆的結果 展開
- 解熱鎮痛抗炎葯-非甾體抗炎藥品類
- 解熱鎮痛抗炎葯
西樂葆
解熱鎮痛抗炎葯-非甾體抗炎藥品類
西樂葆(塞來昔布膠囊,英文商品名為Celebrex),全球第一個上市的選擇性環氧化酶-2抑製劑,隸屬於解熱鎮痛抗炎葯-非甾體抗炎(NSAID)藥品類。與傳統NSAID相比,西樂葆具備較低的消化道不良反應,且鎮痛抗炎療效確切。截止到目前,全球100多個國家地區患者在接受Celebrex治療,各項臨床研究涉及塞來昔布(Celebrex)使用者超過174000例。基於大量的臨床研究證據,它已被國內外多個醫學指南推薦使用。西樂葆在中國被批准用於治療:1)用於緩解骨關節炎的癥狀和體征;2)用於緩解成人類風濕關節炎的癥狀和體征;3)用於治療成人急性疼痛;4)用於緩解強直性脊柱炎的癥狀和體征。
心血管風險
本品可能使嚴重心血管血栓事件、心肌梗塞和中風的風險增加,其風險可能是致命的。所有非甾體抗炎葯(NSAIDs)可能都具有相似的風險。這種風險可能隨藥物使用時間的延長而增加。有心血管疾病或心血管疾病危險因素的患者,其風險更大(見[注直事項]警告和[臨床試驗])。
本品禁用子冠狀動脈搭橋術(CABG)圍手術期的疼痛治療。
胃腸道風險
非甾體抗炎葯(NSAIDs)包括本品。使嚴重胃腸道不良事件的風險增加,包括胃或腸道的出血、潰瘍和穿孔,其風險可能是致命的,這些事件可以發生在用藥期間的任何時間。並且可以沒有譬示癥狀。老年患者發生嚴重胃腸道事件的風險更大。(見[注意事項]警告)
本品主要成份及其化學名稱為:塞來昔布,4-[5-(4-甲苯基)-3-(三氟甲基)-1 氫-1-吡唑-1-基] 苯磺醯胺
化學結構式: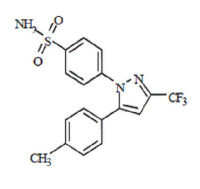

西樂葆
分子式:CHFNOS
分子量:381.38
本品為膠囊劑,內容物為白色粉末。
在決定使用本品前,應仔細考慮本品和其他治療選擇的潛在利益和風險。根據每例患者的治療目標,在最短治療時間內使用最低有效劑量(見[注意事項]-警告)。
1)用於緩解骨關節炎的癥狀和體征。
2)用於緩解成人類風濕關節炎的癥狀和體征。
3)用於治療成人急性疼痛。(見[臨床試驗])
(1)0.1g (2)0.2g
在決定使用本品前,應仔細考慮本品和其他治療選擇的潛在利益和風險。根據每例患者的治療目標,在最短治療時間內使用最低有效劑量(見[注意事項]- 警告)。
骨關節炎和類風濕關節炎,根據個體情況決定本品治療的最低劑量。進食的時間對此使用劑量沒有影響。
骨關節炎:本品緩解骨關節炎的癥狀和體征推薦劑量為200mg,每日一次口服或100mg 每日兩次口服。
類風濕關節炎:本品緩解類風濕關節炎的癥狀和體征推薦劑量為100mg 至200mg,每日兩次。
急性疼痛:推薦劑量為第1 天首劑400mg, 必要時,可再服200mg;隨後根據需要,每日兩次,每次200mg。
特殊人群
肝功能受損患者:中度肝功能損害患者(Child-Pugh II 級)本品的每日推薦劑量應減少大約50%。不建議嚴重肝功能受損患者使用本品(見 [葯代動力學]-特殊人群)。
在臨床對照研究中,已有大約4250 例骨關節炎(OA)患者,2100 例類風濕關節炎(RA)患者和1050例術后疼痛患者接受本品治療。其中超過8500 例患者接受的每日總劑量達200mg(100mg 每日兩次或200mg 每日一次)或更高,包括400 多例患者接受每日總劑量達800mg(400mg 每日兩次)。約有3900 例患者接受上述劑量6 個月或6 個月以上,其中約2300 例患者達一年或一年以上,124 例達2年或2年以上。
由於各個臨床研究的情況不盡相同,直接比較兩種藥物在不同臨床研究中的不良反應發生率是不恰當的,而且臨床研究中的不良反應發生率也可能與臨床實踐中的情況有所不同。但是,臨床試驗中的不良反應信息確實可以為識別不良事件與藥物使用的相關性及估計其發生率提供參考。
上市前的關節炎對照臨床研究中的不良事件:
在涉及安慰劑或陽性藥物對照的12 項臨床研究中,不良事件導致的停葯率在塞來昔布膠囊組是7.1%,在安慰劑組為6.1%。塞來昔布組最常見的因不良事件而停葯的原因是消化不良和腹痛(在接受塞來昔布治療的患者中分別為0.8% 和 0.7%)。安慰劑組0.6%的患者因消化不良而退出研究,因腹痛退出的患者也為0.6%。
關節炎對照研究中塞來昔布膠囊治療組發生率大於2%的不良事件
表1 顯示了在骨關節炎或類風濕關節炎患者中進行的12 項含安慰劑和/或陽性藥物對照的臨床研究中所有塞來昔布膠囊治療組發生率大於2%的不良事件(不論是否與治療有無因果關係)。由於這12 項試驗的研究期限不同,這些試驗中的患者服用藥物的時間不同,所以從這些百分數中不能得到累積發生率。
表1: 上市前的類風濕關節炎對照研究中塞來昔布膠囊治療組發生率大於2%的不良事件
以下為不論是否與治療有因果關係,發生率小於2%(0.1 - 1.9%)的不良事件(患者服用塞來昔布膠囊100- 200mg 每日兩次或200mg 每日一次)。
心血管系統:高血壓加重、心絞痛、冠狀動脈病變、心肌梗死。
全身性:敏感症加重、過敏反應、衰弱、胸痛、非特定囊腫、全身水腫、面部水腫、疲勞、發熱、面部潮紅、感冒樣癥狀、疼痛、周圍疼痛。
男性生殖系統:前列腺疾病。
聽力和前庭:失聰、聽力失常、耳痛、耳鳴。
心率和心律:心悸、心動過速。
肝膽系統:肝功能異常、ALT 升高、AST 升高。
血小板(出凝血)淤癍、鼻出血、血小板增多。
血液系統:貧血。
給葯部位病變:蜂窩組織炎、接觸性皮炎、注射部位反應、皮膚結節。
特殊感覺:味覺錯亂。
以下為不論是否與治療有因果關係, 發生率[0.1%的其它非常罕見的嚴重不良反應
(在服用本品患者中,下列嚴重不良事件極少發生。僅見於上市后病例報道的用斜體字表示。)
肝膽系統:膽石症、肝炎、黃疸、肝衰竭。
腎臟:急性腎衰、間質性腎炎。
皮膚:多型紅斑、剝脫性皮炎、Stevens-Johnson 綜合症、中毒性表皮壞死溶解症。
全身性:膿毒血症、猝死、過敏反應、血管性水腫。
長期、安慰劑對照腺瘤息肉預防研究中的不良反應:在APC 和PreSAP 兩項臨床研究中,塞來昔布用量為400 mg/日至800mg/日,用藥時間長達3 年。(見特殊研究-腺瘤息肉預防研究)。
部分不良反應的發生率高於上市前的關節炎臨床研究(治療持續12 周;參見塞來昔布關節炎上市前臨床對照研究的不良事件)。對比上市前的關節炎臨床研究,塞來昔布治療發生率較高的不良反應如下:
在長期腺瘤息肉預防研究中,塞來昔布治療組以下不良反應的發生率在0.1%--1%之間,高於安慰劑組。同時,這些不良反應在上市前的關節炎對照研究中未被報道,或在上市前的關節炎對照研究中的發生率較低。
神經系統異常:腦梗塞
眼異常:玻璃體漂浮物、結膜出血。
耳及內耳異常:內耳炎。
血管異常:深靜脈血栓。
生殖系統和乳房異常:卵巢囊腫。
實驗室檢查異常:血鉀、血鈉濃度升高、血睾丸酮濃度下降。
損傷,中毒及操作併發症:上髁炎、肌腱斷裂。
CLASS 研究中的安全性數據:
血液系統的事件:
在該項研究中(見特別研究–CLASS),服用本品400mg 每日兩次(分別是骨關節炎(OA)和類風濕關節炎(RA)推薦劑量的4 倍和2 倍,是FAP 的批准劑量)的患者通過複查確定有臨床意義的血紅蛋白降低(]2 g/dL)的發生率低於服用雙氯芬酸75mg 每日兩次或布洛芬800mg 每日三次的患者,分別為0.5%、1.3%和1.9%。無論是否同時服用ASA 本品不良事件的發生率均較低。(見[藥理毒理]–血小板)。
退出研究/嚴重不良事件(SAE):
第9 個月服用本品、雙氯芬酸和布洛芬的患者由於不良事件(AE)退出研究的Kaplan-Meier 累積率分別為 24%、29%和 26%。三個治療組之間嚴重不良事件(SAE,例如:導致住院、威脅生命或其他的有醫學意義的情況)的發生率,無論是否與藥物有因果關係均無差異,分別為8%、7%和8%。
鎮痛和痛經研究中的不良事件:
在鎮痛和痛經研究中大約有1700 例患者接受本品治療。口腔手術后疼痛研究中的所有患者接受單劑量研究藥物。在原發性痛經和骨科手術后疼痛研究中使用本品的劑量最高達600mg/天。在鎮痛和痛經研究中不良事件的類型與關節炎研究中報道的相似。在口腔手術后疼痛研究中唯一增加的不良事件是拔牙后牙槽骨炎(干槽症)。
本品禁用於對塞來昔布過敏者。
本品不可用於已知對磺胺過敏者。
本品不可用於服用阿司匹林或其他非甾體類抗炎葯后誘發哮喘、蕁麻疹或過敏反應的患者。在這些患者中已有非甾體類抗炎葯誘發的嚴重的(極少是致命的)過敏反應報道(見[注意事項] -警告-過敏反應和[注意事項] -注意事項-伴有哮喘)。
本品禁用於冠狀動脈搭橋手術(CABG)圍手術期疼痛的治療(見[注意事項]-警告)。
本品禁用於有活動性消化道潰瘍/出血的患者。
本品禁用於重度心力衰竭患者。
警告
[u]心血管影響[/u]
心血管血栓性事件
長期使用本品可能引起嚴重心血管血栓性不良事件,心肌梗塞和中風的風險增加,其風險可能是致命的,在APC試驗中,與安慰劑相比,本品400mg每日兩次,心源性死亡,心肌梗塞或中風複合終點的相對風險(RR)為3.4(95%CI:1.4-8.5),本品200mg每日兩次的相對風險為2.5(95%CI:1.0-6.4)(見特別研究-腺瘤息肉研究)。
所有非甾體抗炎葯(NSAIDs),包括COX-2選擇性和非選擇性藥品,都可能有類似的風險,已知有心血管疾病或有心血管疾病危險因素的患者,其風險可能更大。為了使接受西樂葆治療的患者發生心血管不良事件的潛在風險最小化,應儘可能在最短療程內使用最低有效劑量,即使既往沒有心血管癥狀,醫生和患者也應對此類事件的發生保持警惕。應告知患者嚴重心血管安全性的癥狀和/或體征以及如果發生應採取的步驟。患者應該警惕諸如胸痛、氣短、無力、言語含糊等癥狀和體征,而且當有任何上述癥狀或體徵發生后該馬上尋求醫生幫助。
尚沒有一致的證據證明,使用NSAID所增加的嚴重心血管血栓性事件的風險,會因同時服用阿司匹林而減輕,同時使用阿司匹林和本品使嚴重胃腸道事件的風險增加(風胃腸道警告)。
在兩項大規模的,對照的臨床試驗中使用其它的COX-2選擇性NSAID治療CABG手術后前10-14天的疼痛,發現心肌梗塞和中風的發生率增加(見[禁忌])。
高血壓
和所有非甾體抗炎葯(NSAIDs)一樣,本品可導致新發高血壓或使已有的高血壓加重,其中的任何一種都可導致心血管事件的發生率增加,服用噻嗪類或髓攀利尿劑的患者服用非甾體抗炎葯(NSAIDs)時,可能會影響這些治療的療效。高血壓病患者應慎用非甾體抗火藥(NSAIDs)包括本品。在開始本品治療和整個治療過程中應密切監測血壓。CLASS試驗中,使用本品,布洛芬和雙氯芬酸治療的患者高血壓的發生率分別為2.4%、4.5%和2.5%(見特別研究-CLASS)。
充血性心力衰竭和水腫
一些服用非甾體抗炎葯(NSAIDs)包括本品的患者出現液體瀦留和水腫(見[不良反應])。在CLASS研究中(見特別研究-CLASS),服用本品400mg每日兩次(分別是骨關節炎(OA)和類風濕關節炎(RA)推薦劑量的4倍和2倍,是FAP的批准劑量)、布落芬800mg每日三次和雙氯芬酸75mg每日兩次的患者第9個月外周水腫的Kaplan-Meier累積率分別為4.5%、6.9%和4.7%,塞來昔布應慎用於有體液瀦留或心衰的患者。
[u]胃腸道(GI)影響—胃腸道潰瘍,出血和穿孔的風險:[/u]
非甾體類抗炎葯(NSAIDs)包括本品,可引起嚴重的可能致命的胃腸道事件,包話胃、小腸或大腸的出血、潰瘍和穿孔。接受非甾體抗炎葯(NSAIDs)治療的患者,這些不良反應可以出現在任何時候,伴或不伴有徵兆。每5例接受NSAID治療發生嚴重的胃腸道不良事件的患者中僅有1例會出現癥狀。在CLASS試驗中所有患者在第9個月複雜性和癥狀性潰瘍的發生率為0.78%,小劑量阿司匹林組為2.19%,第9月時,年齡大於和等於65歲患者的發生率為1.40%,同時服用ASA為3.06%(見特別研究-CLASS)。長期使用非甾體抗炎葯(NSAIDs),在治療過程中發生嚴重胃腸道事件的可能性有增加的趨勢。但是,即使短期治療也不是沒有風險。
既往有胃腸道潰瘍和出血史的患者使用非甾體抗炎葯(NSAIDs)時應特別小心。
既往有消化性潰瘍和/或胃腸出血史的患者,使用非甾體抗炎葯(NSAIDs)發生胃腸出血的危險性比沒有這些危險因素的病人高10倍。增加使用非甾體抗炎葯(NSAIDs)治療的患者胃腸出血危險的其他因素包括同時口服皮質類因醇類藥物或抗凝劑,長期使用非甾體抗炎葯(NSAIDs)治療,吸煙,飲酒,老年齡和一般健康情況差。大部分致命的胃腸道事件的自發報告發生在老年和衰弱的患者,因此治療此類病人時應特別小心。
為使潛在的胃腸道危險性最小化,儘可能使用在最短治療時間內使用最低有效劑量。醫生和患者在本品治療過程中應對胃腸道潰瘍和出血的癥狀和體征保持警惕,如果懷疑發生嚴重胃腸道不良事件,應迅速開始其他的評價和治療,對於高危的患者,應考慮轉換為不含非甾體抗炎葯(NSAIDs)的治療方案。
[u]對肝臟影響[/u]:
在關於非甾體抗炎葯(NSAIDs)的臨床研究中,多至15%的服用非甾體抗炎葯(NSAIDs)的患者會有一項或多項肝臟實驗室指標的臨界增高,約有1%的患者會出現顯著的ALT或AST的升高(三倍或更多倍高於正常值的上限)。繼續治療下,這些實驗室異常值會進展,保持穩定或恢復正常。在非甾體抗炎葯(NSAIDs),包括本品的治療中,有罕見的嚴重肝臟反應的報道(見[不良反應]上市後用葯經驗),包括黃疸型和致命的暴髮型肝炎,肝壞死和肝功能衰竭(有些將會致命)。在本品對照臨床研究中,肝臟實驗室指標的臨界增高的發生,在塞來昔布膠囊治療組為6%,安慰劑組為5%;出現顯著的ALT或AST的升高,在塞來昔布膠囊治療組為0.2%而安慰劑組為0.3%。
若服用本品的患者也有提示肝臟功能不全的癥狀和/或體征,或有肝臟功能不全的實驗室證據,應仔細觀測肝臟功能惡化發展的證據。若癥狀和體征均提示肝臟疾病進展,或有全身表現(如:嗜酸細胞增多症,皮疹等)應停用塞來昔布。
[u]腎臟影響[/u]
長期使用非甾體抗炎葯(NSAIDs)會導致腎乳頭壞死和其他的腎臟損害。有毒性也見於腎臟灌注維持中前列腺素起補償作用的患者。在這些患者中,使用NSAID會導致前列腺素生成的劑量依賴性減少,隨之發生腎血流量減少,這將促成明顯的腎臟失代償。此類風險最高的患者是腎功能不全、心力衰竭、肝功能不全的患者,使用利尿劑和ACE抑製劑的患者和老年患者。停用非甾體抗炎葯(NSAIDs)后,通常可恢復至治療前的狀況。臨床試驗顯示,本品對腎臟的影響與對照的非甾體抗炎葯(NSAIDs)相似。
在現有的對照臨床研究中,尚無在進展期腎臟疾病的患者中應用本品的資料。故不推薦在進展期腎臟患者中應用本品。如必須使用本品,建議密切監測患者的腎功能。
[u]過敏反應[/u]
與一般的非甾體類抗炎藥物相同,在未服用過本品的患者中也可以發生過敏反應。上市後用葯經驗表明,服用本品的患者極少發生過敏反應和血管性水腫。本品不應用於有阿司匹林三聯症的患者。這些症侯群特徵性地出現在有鼻炎的哮喘患者伴或不伴鼻息肉,或出現在服用阿司匹林或其它非甾體類抗炎藥物后出現嚴重的,潛在致命的支氣管痙攣的患者(見[禁忌]和[注意事項]-伴有哮喘)。如發生過敏反應應進行急診治療。
[u]皮膚反應[/u]
本品一種磺胺類藥物,可引起可能致命的,嚴重的皮膚不良反應。例如剝脫性皮炎、Stevcns Johnson綜合征(SJS)和中毒性表皮壞死溶解症(TENS)。這些嚴重事件可在沒有徵兆的情況下和既往未知對磺胺過敏的患者中出現。應告知患者嚴重皮膚反應的癥狀和體征,在第一次出現皮膚皮疹或過敏反應的任何其他徵象時,應停用塞來昔布。
[u]妊娠期[/u]
在妊娠晚期應避免使用本品,因為這將導致動脈導管提前閉合。(見[孕婦及哺乳期婦女用藥])
[u]皮質類固醇激素治療[/u]
塞來昔布不能用來替代皮質類固醇激素或治療皮質類固醇激素缺乏。驟然停用皮質類固醇激素會導致需皮質類固醇激素控制的疾病的惡化。長期使用皮質類固醇激素治療的患者如決定停葯,則應逐漸減量。
[u]對血液系統的影響[/u]:使用本品治療的患者中有時會出現貧血。在臨床對照研究中,貧血的發生率在塞來昔布膠囊治療組為0.6%,在安慰劑組為0.4%。長期應用本品的患者出現任何貧血或失血的癥狀和體征應該檢查血紅蛋白和血細胞比容。按規定劑量使用塞來昔布膠囊一般不影響血小板的計數,凝血酶原時間(PT)或部分凝血活酶時間(PTT),不影響血小板聚集(見[藥理毒理]-血小板)。
[u]彌散性血管內凝血[/u]
鑒於有發生彌散性血管內凝血的風險,將塞來昔布用於全身型幼年類風濕關節炎患者時應謹慎。
[u]伴有哮喘[/u]
哮喘患者可能因阿司匹林過敏而誘發哮喘。有阿司匹林誘發哮喘的患者使用阿司匹林會導致嚴重的可能致命的支氣管痙攣。由於這些阿司匹林過敏的患者中阿司匹林和其它NSAIDs 之間的交叉反應(包括支氣管痙攣)已有報道,故塞來昔布不應用於此類型的阿司匹林過敏患者,在伴有哮喘的患者中應用塞來昔布也要謹慎。
其他注意事項
[u]實驗室檢查[/u]
因為嚴重的胃腸道潰瘍和出血會在沒有任何徵兆的情況下發生,醫生應監測發生胃腸道出血的癥狀及體征。長期使用N S A I D s 治療的患者,應定期進行全血細胞計數( CBC)和血生化檢查。如果肝功能或腎功能異常持續存在或加重,應停用塞來昔布。
對照臨床研究顯示,接受塞來昔布治療的患者中高氯血症的發生率高於使用安慰劑的患者。其他在服用塞來昔布患者較安慰劑更多見的實驗室檢查異常包括低磷酸鹽血症和BUN 的升高。這些實驗室檢查異常也見於在這些臨床研究中接受NSAIDs 對照治療的患者中。這些異常的臨床意義尚未確定。
[u]炎症[/u]
假定非感染性疼痛與感染合併存在時,塞來昔布減輕炎症和可能緩解發熱的藥理學特性會減弱這些陽性體征在診斷感染上的價值。
[u]合併使用NSAIDs[/u]
由於可能增加不良反應發生的風險,應避免與任何劑量的其他NSAIDs合併使用。
患者須知:
在開始本品治療和治療過程中應定期告知患者以下信息。
1、本品與其它非甾體抗炎葯(NSAIDs)一樣,可能引起嚴重的心血管副作用,例台心肌梗塞或中風,這些副作用可能導致住院甚至死亡。雖然嚴重心血管事件的發生可能沒有任何徵兆,但是患者應警惕胸痛、呼吸短促、乏力、言語含糊的癥狀和體征,如果出現這些癥狀或體征,應尋求醫療幫助。應告知患者隨診的重要性(見[注意事項]-警告–對心血管影響)。
2、本品與其它非甾體抗炎葯(NSAIDs)一樣,可能想起胃腸道不適,罕見而更嚴重的副作用如潰瘍和出血會,可能導致住院甚至死亡。雖然嚴重的胃腸道潰瘍和出血的發生可能沒有任何徵兆,但是患者應警惕潰瘍和出血的癥狀和體征,在發現任何預示這些疾病的癥狀和體征包括腹上部疼痛、消化不良、黑便和嘔血時,應尋求醫療幫助。應告知患者隨診的重要性(見[注意事項]-警告-胃腸道(GI)影響–上消化道潰瘍、出血和穿孔的風險)。
3、應告知患者,如果出現任何類型的皮疹,應立即停葯,並儘快與醫生聯繫。本品是一種磺胺類藥物,可以引起導致住院甚至死亡的嚴重的皮膚副作用,例如剝脫性皮炎、Stevens Johnson綜合征和中毒性表皮壞死溶解症(TENS)。所有的、甚至是非磺胺類非甾體抗炎葯(NSAIDs)都可能發生這些反應。雖然嚴重的皮膚反應的發生可能沒有徵兆,但是患者應警惕皮疹和水皰的癥狀和體征、發熱或過敏反應的其他體征如搔癢,在發現任何徵兆的癥狀或體征時,應尋求醫療幫助。既往有磺胺過敏史的患者不應服用塞來昔布。
4、患者應迅速向醫生報告無法解釋的體重增加或水腫的癥狀和體征。
5、應告知患者預示肝臟毒性反應的癥狀和體征(如:噁心、疲勞、嗜睡、瘙癢、黃疸、右上腹痛和“感冒樣”癥狀)。如發生這些癥狀和體征,應停止用藥,並立即尋求治療(見[注意事項]-警告-過敏反應)。
6、應告知患者過敏反應的癥狀和體征(如呼吸困難、顏面或喉部水腫)。如果發生這些癥狀或體征,應停止用藥,並立即尋求治療(見[注意事項]-警告-過敏反應)。
7、因為導致動脈導管提前閉合,在妊娠晚期應避免使用塞來昔布。
致畸作用:
妊娠期分級C 級。在口服劑量150mg/kg/day 時(按AUC0-24計,暴露劑量約與臨床劑量200mg每日兩次的2 倍相當),可觀察到胚胎異常的發生率增加,如:肋骨融合,胸骨節融合和胸骨節畸形。在兩項關於大鼠的研究中,其中一項研究發現在口服劑量30mg/kg/天時(按AUC0-24計,暴露劑量約與臨床劑量200mg 每日兩次的6 倍相當),有劑量依賴的膈疝發生的增加。沒有妊娠婦女應用本品的研究。只有當考慮潛在的益處大於對胎兒的危害時才可考慮在妊娠期使用塞來昔布。
非致畸作用:
大鼠在口服塞來昔布劑量50mg/kg/天時(按AUC0-24計,暴露劑量約與臨床劑量200mg 每日兩次的6 倍相當),會導致著床前、著床后流產和胚胎存活率的降低。此種作用是由於抑制前列腺素合成所致,對生殖功能並無永久的影響,在臨床正常應用下不會發生此類情況。目前尚無本品對動脈導管閉合作用的人體研究評估資料。所以在懷孕的后3 個月內要避免使用塞來昔布。
分娩和生產:
大鼠在口服塞來昔布劑量高達100mg/kg 時(相當於按AUC0-24人體在200mg 每日兩次時暴露劑量的約7 倍),無證據表明其有延遲分娩和生產作用。本品對妊娠期婦女分娩和生產的影響尚不清楚。
哺乳期:
在哺乳大鼠中進行的研究顯示塞來昔布能經乳汁分泌,濃度和血漿濃度相似。塞來昔布能否經哺乳婦女的乳汁分泌尚不清楚。由於許多藥物會經哺乳婦女的乳汁分泌和塞來昔布膠囊可能會對哺乳期嬰幼兒引發潛在的嚴重不良反應,故應根據藥物對母親重要性的考慮,決定是否停止哺乳或停止用藥。
目前尚無關於18 歲以下兒童應用塞來昔布的療效和安全性的資料。
在各臨床研究接受本品治療的全部患者中,有超過3300 例是65-74 歲的患者,而有約1300 例是75 歲以上的。老年患者和年輕患者在藥物的療效和安全性方面未見明顯的差異。
在以腎小球濾過率(GFR),BUN 和肌酐檢測腎功能,以出血時間,和血小板聚集試驗檢測血小板功能的臨床研究中,發現在老年和年輕的志願者中無差異。但是,服用其他非甾體抗炎葯(NSAIDs),包括選擇性COX-2 抑製劑,老年患者發生致命性胃腸道事件和急性腎功能衰竭的自發性上市后報告多於年輕患者。(見[注意事項]-警告–胃腸道 (GI) 影響 –消化道潰瘍、出血和穿孔的風險)。
一般情況:
當塞來昔布與有抑制P450 2C9 作用的藥物同時服用時,會產生明顯的藥物相互作用。體外的研究提示:塞來昔布不是細胞色素P450 2C9,2C19 或 3A4 的抑製劑。
臨床研究發現:塞來昔布與氟康唑和鋰之間有潛在明顯藥物相互作用。來自非甾體抗炎葯(非甾體抗炎葯(NSAIDs))的經驗提示:與速尿和血管緊張素轉化酶抑製劑(ACE)抑製劑有潛在的相互作用。研究了塞來昔布在體內與優降糖,酮康唑,甲氨喋呤,苯妥英和甲苯磺丁脲的葯代動力學和藥效學,未發現有重要臨床意義的藥物相互作用。
通常:
塞來昔布主要經肝臟細胞色素P450 2C9 代謝。當塞來昔布與有抑制2C9 作用的藥物同時服用時應加註意。
體外研究表明:儘管塞來昔布不是P450 2D6 的底物但是其的抑製劑。所以其在體內有可能與需要經P450 2D6 代謝的藥物發生相互作用。
ACE-抑製劑和血管緊張素Ⅱ拮抗劑:
有報道提示非甾體抗炎葯(NSAIDs)會減弱血管緊張素轉化酶(ACE)抑製劑和血管緊張素Ⅱ拮抗劑的抗高血壓作用。在同時服用ACE-抑製劑、血管緊張素Ⅱ拮抗劑和塞來昔布膠囊的患者中要考慮這種藥物相互作用。
速尿:
臨床研究和上市后監測顯示:非甾體抗炎葯(NSAIDs)在一些患者中會降低速尿和噻嗪類利尿藥物的促尿鈉排泄作用。這與腎臟的前列腺素合成被抑制有關。
阿司匹林:
本品可以和低劑量的阿司匹林合用。然而與單獨使用本品相比,同阿司匹林聯合使用時胃腸道的潰瘍和其他併發症的發生率會增加(見[臨床試驗]-特別研究- CLASS,[注意事項]- 警告–胃腸道(GI))影響 –消化道潰瘍、出血和穿孔的風險和警告-心血管影響)。由於缺乏對血小板的作用,本品不能替代阿司匹林在預防心血管事件方面的治療。
氟康唑:
同時服用氟康唑200mg 每日一次,塞來昔布的血葯濃度升高兩倍。這是由於塞來昔布經P450 2C9的代謝被抑制(見[藥物代謝動力學]-代謝)。接受氟康唑治療的患者應給予本品最低的推薦劑量。
鋰:
在健康受試者中進行的研究表明:同時服用鋰450mg 每日兩次和本品200mg 每日兩次的受試者中,鋰穩態血漿濃度較單用鋰的受試者升高了約17%。對接受鋰治療的患者在開始使用和停用本品時,須密切觀察。
甲氨喋呤:
在一項類風濕關節炎患者服用甲氨喋呤的交叉設計的研究中,塞來昔布膠囊對甲氨喋呤的葯代動力學無明顯影響。
華法林:
接受華法林或其它類似藥物治療的患者,特別在開始服用本品的數天內或改變其劑量時,因為患者發生出血併發症的危險性增高,要監測患者的抗凝血活性。在一組每日服用2-5mg 華法林的健康受試者中研究了塞來昔布對華法林抗凝作用的影響。在這些受試者中,通過凝血酶原時間測定證明塞來昔布不影響華法林的抗凝作用。而據上市後用葯經驗的報道:合用塞來昔布和華法林的患者中(主要是老年人)會有因凝血酶原時間延長而導致出血事件發生。
在臨床研究中沒有服用本品過量的報告。12 例患者服用劑量高達2400mg/天,共10 天,沒有引起嚴重的毒性。急性NSAID 過量的癥狀通常限於疲倦、嗜睡、噁心、嘔吐和上腹痛,經支持治療后一般會緩解。亦會有胃腸道出血。罕見的有:高血壓、急性腎衰、呼吸抑制和昏迷。治療劑量下有過敏反應的報道,故過量時也可能出現。
NSAID 過量后應對症處理和支持治療。沒有特效的解毒劑。沒有關於以血液透析去除塞來昔布的研究資料,但由於其血漿蛋白結合率高,過量時透析療法可能無效。病人過量服藥后4 小時內如無癥狀或過量很大時,也可用藥物催吐,和/或活性炭(成人60-100g,兒童1-2g/kg ),和/或滲透性導瀉等方法救治。由於蛋白結合率高,利尿、鹼化尿液、血液透析或血液超濾可能無效。
西樂葆
本品與安慰劑相比能顯著減輕關節疼痛。在幾項為期最長達12 周、安慰劑和陽性藥物對照的臨床研究中評價了本品對膝關節炎和髖關節炎癥狀和體征的治療。本品100mg 每日兩次或200mg 每日一次,改善了OA 患者的WOMAC(Western Ontario and McMaster Universities)骨關節炎指數(關於OA的關節疼痛,僵硬和功能的綜合評價指標)。在三項為期12 周,OA 發作伴隨疼痛的研究中,本品100mg 每日兩次和200mg 每日兩次能在給葯后的24-48 小時內明顯減輕疼痛。本品100mg 每日兩次或200mg 每日兩次其療效與萘普生500mg 每日兩次相似。200mg 每日兩次的劑量與100mg 每日兩次相比未發現更明顯的優勢。當本品每日總劑量為200mg 時,以100mg 每日兩次或以200mg 每日一次的方式服用的療效等效。
類風濕關節炎:
本品與安慰劑相比能顯著減輕關節觸痛/疼痛和關節腫脹。在幾項為期最長達24 周、安慰劑和陽性藥物對照的臨床研究中評價了本品對RA 癥狀和體征的療效。ACR20 反應指數(關於RA 的臨床,實驗室和功能的綜合評價指標),顯示本品優於安慰劑。本品100mg 每日兩次和200mg 每日兩次的療效相似,且與萘普生500mg 每日兩次療效相當。
雖然本品100mg 每日兩次和200mg 每日兩次的總體療效相似,但有些患者在200mg 每日兩次中獲得更多的益處。400mg 每日兩次未見較100-200mg 每日兩次更多的益處。
鎮痛作用,包括原發性痛經:
在口腔術后疼痛、骨科術后疼痛和原發性痛經的急性鎮痛模型中,本品可緩解患者中度到重度的疼痛。單劑量(見[用法用量])本品在60 分鐘內可緩解疼痛。
特別研究
塞來昔布長期關節炎安全性研究(CLASS)
塞來昔布長期關節炎安全性研究(CLASS)是一項在大約5800 例骨關節炎和2200 例類風濕關節炎患者中進行的上市后的前瞻性長期安全性終點研究。患者接受塞來昔布400mg 每日兩次(分別為骨關節炎和類風濕關節炎推薦劑量的4 倍和2 倍)、或布洛芬800mg 每日三次、或雙氯芬酸75mg 每日兩次(常用的治療劑量)。塞來昔布(n=3987)和雙氯芬酸(n=1996)平均使用9 個月,布洛芬(n=1985)6 個月。該研究的主要終點是複雜性潰瘍(胃腸道出血、穿孔或梗阻)的發生率。允許患者同時服用小劑量(≤325mg/d)阿司匹林預防心血管疾病(阿司匹林亞組:塞來昔布,n=882;雙氯芬酸,n=445;布洛芬,n=412)。塞來昔布複雜性潰瘍的發生率與布洛芬和雙氯芬酸兩組之和沒有統計學意義。
那些同時服用塞來昔布和小劑量阿司匹林(N=882)的患者複雜性潰瘍的發生率比未用阿司匹林(N=3105)患者高4 倍。在9 個月時,服用小劑量阿司匹林和未服用小劑量阿司匹林複雜性潰瘍的Kaplan Meier 比率分別為1.12%和0.32%(見[注意事項]- 警告-胃腸道(GI)影響-消化道潰瘍、出血和穿孔的風險)。
使用塞來昔布400mg 每日兩次 9 個月時發生複雜性和癥狀性潰瘍的估計累積率見表2。表2 還展示了年齡小於或大於65 歲患者的結果。可能是使用阿司匹林者發生胃腸道事件的風險更高而導致了塞來昔布單獨使用組和塞來昔布與阿司匹林合併使用組之間發生率的差異。
表2. 根據危險因素,服用塞來昔布400mg BID 患者9 個月時複雜性和癥狀性潰瘍的發生率(Kaplan-Meier 比率[%])
在少數有潰瘍病史的患者中,單獨服用塞來昔布或塞來昔布與阿司匹林同時服用的患者在48 周時發生複雜性和癥狀性潰瘍的比例分別為2.56%(n=243)和6.85% (n=91)。這些結果在既往有潰瘍病史的患者中時是預期的(見[注意事項]- 警告-胃腸道(GI)影響-胃腸道潰瘍、出血和穿孔的風險和[不良反應]-CLASS 研究中的安全性資料-血液系統的事件)。
心血管安全性也在CLASS 試驗中得到了評價。研究者報告的嚴重心血管血栓栓塞性不良事件(包括心肌梗死、肺動脈栓塞、深靜脈血栓、不穩定心絞痛、短暫性缺血發作和缺血性腦血管事件)的Kaplan-Meimer 累積率證實,在塞來昔布、雙氯芬酸和布洛芬治療組之間沒有差異。在9 個月時所有塞來昔布、雙氯芬酸和布洛芬患者的累積率分別為1.2%、1.4%和1.1%。在9 個月時3 個治療組未使用阿司匹林患者的累積率均小於1%。在9 個月時3 個治療組未使用阿司匹林患者心肌梗死累積率均小於0.2%。在CLASS 試驗中沒有安慰劑組,限制了確定這3 種受試藥物是否不增加心血管事件的風險或增加風險的程度相似。
腺瘤息肉預防研究
在兩項塞來昔布治療散發性腺瘤息肉的隨機、雙盲、安慰劑對照、為期3 年的研究中評價了心血管安全性。第一項研究是APC 試驗,塞來昔布400mg 每日兩次(N=671)和200mg 每日兩次(N=685)與安慰劑(N=679)比較。該試驗初步的安全性信息證實,與安慰劑相比,塞來昔布200mg 每日兩次和400mg每日兩次,嚴重心血管事件呈劑量相關性增加(主要為心肌梗死)。大約治療1 年後塞來昔布治療組和安慰劑組之間嚴重心血管血栓事件的累積率開始有差異。除早期死亡的患者外,APC 試驗的隨訪時
間為2.8~3.1 年。與安慰劑相比,心源性死亡、心肌梗死或卒中複合終點的相對風險(RR)在塞來昔布高劑量組為3.4(95%CI:1.4~8.5),低劑量組為2.5(95%CI:1.0~6.4)。複合終點的絕對風險在塞來昔布高劑量組為3.0%,低劑量組為2.2%,安慰劑組為0.9%。
第二項長期研究PreSAP 研究,比較塞來昔布400mg 每日一次和安慰劑。該研究初步的安全性信息證實,心血管死亡、心肌梗死或卒中複合終點的心血管風險沒有增加。導致塞來昔布APC 試驗和PreSAP 試驗心血管事件結果不同的原因尚不清楚。
最長達3 年的其他COX-2 選擇和非選擇性NSAIDs 的臨床試驗顯示,嚴重心血管血栓事件、心肌梗死和卒中的風險增加,其風險可能是致命的。結果認為所有的NSAIDs 均與這種風險有潛在的關係。
內窺鏡研究
塞來昔布短期內窺鏡研究的發現與長期使用有臨床意義的嚴重上胃腸道事件相對發生率之間的關係尚未建立。
在一項430 例類風濕關節炎患者的隨機、雙盲研究中, 6 個月時進行內窺鏡檢查。服用塞來昔布200mg 每日兩次的患者內窺鏡下潰瘍的發生率為4%,服用雙氯芬酸緩釋劑75mg 每日兩次的患者發生率為15%。但是,在CLASS 試驗中,與雙氯芬酸相比,塞來昔布的臨床相關胃腸道終點沒有統計學差異(見特別研究-CLASS)。
在兩項12 周、安慰劑對照試驗中對2157 例骨關節炎和類風濕關節炎患者進行了內窺鏡下潰瘍發生率的研究,這些患者基線內窺鏡檢查未發現潰瘍。胃十二指腸潰瘍發生率與塞來昔布(50mg 至400mg每日兩次)之間沒有劑量相關性。在這兩項研究中萘普生500mg 每日兩次的發生率分別為16.2%和17.6%,安慰劑分別為2.0%和2.3%,塞來昔布所有劑量的發生率為2.7%~5.9%。至今尚未進行大規模的臨床研究以比較塞來昔布和萘普生臨床相關胃腸道終點。
在內窺鏡研究中,大約11%患者服用阿司匹林(≤325mg/d)。在塞來昔布組中,使用阿司匹林者內窺鏡下潰瘍發生率高於未使用者。但是,這些使用阿司匹林者潰瘍發生率的增加少於同時服用或不服用阿司匹林的陽性對照組。
在對照和開放性試驗中均觀察到使用塞來昔布的患者發生嚴重的有臨床意義的上胃腸道出血(見特別研究-CLASS 和[注意事項]- 警告-胃腸道(GI)影響-消化道潰瘍、出血和穿孔的風險)。
作用機理:
本品是非甾體類抗炎葯,動物模型中觀察到其有抗炎、鎮痛和退熱的作用。本品的作用機理是通過抑制環氧化酶-2(COX-2)來抑制前列腺素生成。且在人體治療濃度下,本品對同工酶—環氧化酶-1(COX-1)沒有抑制作用。在動物結腸腫瘤模型中塞來昔布減緩了腫瘤的發生和進展。
臨床藥理:
血小板
在健康志願者的臨床試驗中,本品單劑量最高達800mg 和多劑量600mg 每日兩次,最長達7 天(高於推薦的治療劑量),對血小板聚集的減少或出血時間的延長沒有影響。因為沒有對血小板的作用,本品不能作為阿司匹林的替代品用於預防心血管疾病。本品對血小板是否有任何作用可能增加與本品有關的嚴重心血管血栓性不良事件風險,尚不清楚。
液體儲留
致癌作用,誘導突變,生殖損害:
塞來昔布在大鼠口服劑量高達200mg/kg(雄性)和10mg/kg(雌性)時(按曲線下面積AUC0-24計,暴露劑量與臨床劑量約200mg 每日兩次的2-4 倍相當),或在小鼠口服劑量高達25mg/kg(雄性)和 50mg/kg(雌性)時(按AUC0-24 計,暴露劑量與臨床劑量約200mg 每日兩次相當)服用兩年,未發現有致癌作用。
塞來昔布在中華倉鼠卵巢(CHO)細胞中進行的艾姆斯(Ames)實驗和突變實驗中,未見有誘導突變的作用。在CHO 細胞中進行的染色體畸變實驗和在大鼠體內骨髓中進行的微核實驗中,未見有基因突變的作用。
塞來昔布在口服劑量高達600mg/kg/日時,對雄性和雌性大鼠的生殖功能沒有損害(按AUC0-24計,暴露劑量約與臨床劑量200mg 每日兩次的11 倍相當)。
西樂葆
口服單劑量塞來昔布后約3 小時達最高血葯濃度。在空腹狀態下,塞來昔布劑量高至200mg 每日兩次時,其最高血葯濃度(Cmax)和曲線下面積(AUC)均與劑量大致成正比;劑量再增高時,這種正比關係減弱(見食物影響)。目前,尚未進行絕對生物利用度的研究。多劑量給葯后,5 天內可達到穩態血葯濃度水平。
表1 是塞來昔布在一組健康受試者中的葯代動力學參數。
食物影響
本品與高脂食物同服,會延遲1 至2 小時達最高血葯濃度,同時總體吸收(AUC)會增加10%到20%。在空腹狀態下,劑量超過200mg 時,可能由於其在水性溶液中溶解度低,故Cmax 和AUC 與劑量成正比增加的關係均減弱。本品與抗酸劑(鋁劑和鎂劑)同服,其血葯濃度會降低,Cmax 下降37%而AUC 下降10%。本品劑量高至200mg 每日兩次時,服藥時間不受進食時間的影響。高劑量400mg 每日兩次時應與食物同服以增加吸收。
健康受試者服用本品膠囊與服用本品膠囊內容物混合蘋果泥的整體系統暴露(AUC)相同。本品膠囊內容物與蘋果泥混合后服用,Cmax, Tmax 和 T1/2 均無明顯改變。
分佈
健康受試者在治療劑量下,塞來昔布的血漿蛋白結合高,可達97%。體外研究顯示塞來昔布主要與白蛋白結合,其次與α1 酸糖蛋白結合。穩態血葯濃度水平時表觀分佈容積(Vss/F)為400L,提示塞來昔布在組織中廣泛分佈。塞來昔布並不優先與紅細胞結合。
代謝
塞來昔布主要經細胞色素P450 2C9 代謝。已證實其在人體血漿中的三種代謝產物,醇、相應的羧基酸和其葡糖苷酸結合物。這些代謝產物沒有抑制COX-1 或 COX-2 的活性。根據病史在已知或懷疑有P450 2C9 代謝酶缺乏的患者,應慎用塞來昔布,因為代謝清除的減低會導致塞來昔布的血葯濃度異常增高。
排泄
塞來昔布的清除主要通過肝臟進行代謝,僅有少於3%劑量的藥物以原型從尿和糞中排出。服用單劑同位素標記的藥物后,57%從糞中排出,27%從尿中排出。尿和糞中排出的絕大多數代謝產物是羧基酸(劑量的73%),少量的葡糖苷酸從尿中排出。由於藥物溶解度低使吸收過程延長,導致藥物半衰期(t1/2)差異較大。空腹情況下,有效半衰期約為11 小時。表觀血漿清除率 (CL/F) 約為500 ml/min。
特殊人群
老年人:
在老年人群(大於65 歲)中,塞來昔布的Cmax 和AUC 較年輕人群分別增加40%和50%。老年女性中塞來昔布的Cmax 和AUC 比老年男性高,但這種增高最主要與老年女性體重較低相關。老年人群中,一般不需要對塞來昔布的劑量進行調整。然而對體重低於50 kg 的患者,開始治療時建議使用最低推薦劑量。
兒童:
本品沒有在18 歲以下人群中進行過臨床研究。
人種:
多項葯代動力學研究的薈萃分析提示:與白種人相比,黑種人中塞來昔布的AUC 大約增加40%。其原因和由此產生的臨床意義尚不明確。
肝功能不全:
在輕度肝功能損害(Child-Pugh Class I)患者和中度肝功能損害(Child-Pugh Class II)患者中進行的葯代動力學研究表明:塞來昔布的穩態AUC 較健康受試者分別增高為40%和180%。故在中度肝功能損害(Child-Pugh Class II)的患者中,塞來昔布每日推薦劑量應減少約50%。未在重度肝功能損害的患者中進行有關研究。不推薦在重度肝功能損害的患者中使用塞來昔布。(見[用法用量])
腎功能不全:
一項交叉設計的研究顯示:在慢性腎功能不全的患者(腎小球濾過率(GFR)35-60ml/min)中,塞來昔布的AUC 較腎功能正常者減少約40%。沒有發現GFR 和塞來昔布清除之間存在明顯的相關。未在嚴重腎功能不全的患者中進行有關研究。(見[注意事項]-警告-進展期腎臟疾病)
雖然NSAID已被臨床廣泛用於解熱鎮痛抗炎治療,但直到19世紀70年代,人們才發現此類藥物是通過抑制環氧化酶(COX),阻斷前列腺素生成,而發揮藥理作用的。這一發現者英國藥理學家John Vane也因此獲得了1982年諾貝爾醫學獎。
1991年,科學家們證實,人體內有兩種不同的COX存在。COX-2在組織損傷后產生的,它介導合成的前列腺素導致機體發熱、炎症和疼痛產生。而COX-1則維持細胞正常活性,具有保護胃腸黏膜、維持腎功能、維持血小板功能的作用。傳統NSAID同時抑制兩種COX,胃腸道不良反應多。1998年,首個選擇性COX-2抑製劑塞來昔布(西樂葆)誕生。
1998年12月,西樂葆獲得美國食品藥品監督管理局(FDA)的批准上市,治療骨關節炎、類風濕關節炎,此後又獲得了2歲以上兒童類風濕關節炎、強直性脊柱炎、急性疼痛和原發性痛經的適應症。
2001年1月,西樂葆獲得中國食品藥品監督管理局(CFDA)的批准上市。
2004年,全球第二個選擇性COX-2抑製劑羅非昔布因心血管不良事件在美國撤市。2005年FDA召開顧問委員會會議評估NSAID心血管安全性。FDA認為,多數證據表明常規應用塞來昔布,或對高齡患者應用塞來昔布,心血管風險與非特異NSAIDs相似。顧問委員會以31:1的投票結果支持塞來昔布繼續使用。
2010年,柳葉刀雜誌發表CONDOR研究結果,在骨關節炎和類風濕關節炎患者中比較塞來昔布與傳統NSAID雙氯芬酸聯合質子泵抑製劑奧美拉唑的消化道安全性。揭示雙氯芬酸加奧美拉唑組具有臨床意義的胃腸道不良事件發生率是塞來昔布組的4倍。為塞來昔布消化道安全性提供了高質量的循證證據支持。
密閉,25℃ 以下保存。
鋁塑包裝,2 粒/盒;6 粒/盒;10 粒/盒。
36 個月
進口藥品註冊標準JX20000001
進口藥品註冊證號
(1) 0.1g:H20120356;H20120353
(2) 0.2g:H20120355;H20120354
【分包裝批准文號】
(1) 0.1g:國葯准字J20120062
(2) 0.2g:國葯准字J20120063
Pfizer Pharmaceuticals LLC
輝瑞製藥有限公司
2007年03月06日
2009年05月27日 2012年01月11日 2012年04月16日 2012年11月06日
